工业上利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰的常见流程如下:
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
| pH |
5.2 |
3.2 |
9.7 |
10.4 |
(1)一氧化锰用硫酸酸浸时发生的主要反应的离子方程式为____________________。酸浸后加入MnO2将溶液中的Fe2+氧化成Fe3+,其目的是___________。
(2)滤渣A的成分除MnO2外,还有_______________。
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为________。工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为_________,当阴极产生4.48L(标况)气体时,MnO2的理论产量为______g。
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是_______>_______>_______(填写化学式)。
计算
(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比
是,原子数之比是,质量之比是,密度之比是
(2)下列所给出的几组物质中:含有分子数最多的是;含有原子数最多的
是;标准状况下体积最大的是。
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏加德罗常数,如果ag某气体含有的分子数是b,则cg该气体在
标准状况下的体积是(用含NA的式子表示)。
(4)配制100 mL 1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的
浓H2SO4(密度为1.84g/cm3)的体积为。
A、B、C、D、E、F是原子序数依次增大的六种常见元素。E的单质在C2中燃烧
的产物可使品红溶液褪色。F和C元素形成的化合物F3C4具有磁性。A的单质在C2中燃烧
可生成AC和AC2两种气体。D的单质是一种金属,该金属在AC2中剧烈燃烧生成黑、白两
种固体。请回答下列问题:
⑴B的单质分子的电子式为;F3C4的化学式为;
F元素在周期表中的位置是_____________。
⑵写出D在AC2剧烈燃烧生成黑白两种固体的化学反应方程式
⑶A、B、C形成的10电子氢化物中,A、B的氢化物沸点较低的是(写化学式)____________;
B、C的氢化物分子结合H+能力较强的是(写化学式)______________,用一个离子
方程式加以证明____________________________。
⑷EC2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体BC,有关反应的离
子方程式为__________________________________________,由此可知BC2和EC2还
原性较强的是(写化学式)______________________________。
A、B、C、D、E是常见的几种粒子,其中A、B为分子,C、E为阳离子,D为阴
离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种粒子反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:A:;B :;C:;D :(2)写出A、B、E三种微粒反应的离子方程式:
海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验
室里从海洋中提取碘的流程如下:
⑴指出提取的过程中有关实验操作名称:①;③;
⑵提取碘的过程中,可供选择的溶剂是__________。
| A.酒精 | B.四氯化碳 | C.乙酸 | D.苯(E)水 |
⑶从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出下图所示实验装置中的错误之处;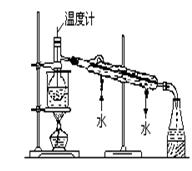
① ; ②;③。
(4)进行上述蒸馏操作时,使用水浴的原因是;最后碘晶在里聚集。
含有下列离子的五种溶液①Ag+ ②Mg2+ ③Al3+ ④ Fe2+ ⑤Fe3+ 试回答下列问题:
(1)既能被氧化又能被还原的离子是____________(填离子符号,下同)
(2)向④中加入NaOH溶液,现象是有关化学方程式为
、。
(3)加入过量NaOH溶液无沉淀的是_____________
(4)加铁粉溶液质量增重的是_________,溶液质量减轻的___________
(5)遇KSCN溶液呈红色的是_________________________
(6)能用来鉴别Cl–存在的离子是___________