如图所示的实验装置可用来测定含两种元素的某种气体X的分子式。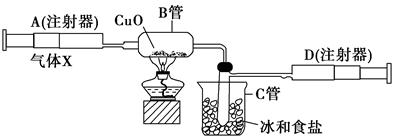
在注射器A中装有240 mL气体X并慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到以下实验结果:实验前B管重20.32 g,实验后B管重20.00 g,B管中的黑色粉末变成红色粉末。在C管中收集到的无色液体是水;在注射器D中收集到的气体是氮气。试回答下列问题:
(1)X气体是由________和________元素组成的。
(2)若240 mL X气体完全反应后,收集到的氮气质量是0.28 g。根据实验时温度和压强计算1 mol X气体的体积是24 000 mL,则X的摩尔质量是________。
(3)通过计算,确定X的分子式为________。
(4)写出B中发生反应的化学方程式(X在该条件下不发生分解反应)________________________。
(8分)现有A、B、C、D四种溶液,它们的阳离子和阴离子均各不相同,所含阳离子是:Ba2+、Ag+、H+、Na+,所含阴离子是:CO32—、NO3—、Cl—、OH-,为了确定这四种溶液成分,进行如下化学实验:
(1)A与B混合后无现象
(2)B与D混合后产生气体
(3)B与C混合后产生沉淀
(4)A与D混合产生沉淀,该沉淀溶于B
(5)A与C混合产生沉淀
| A |
B |
C |
D |
|
| A |
— |
↓ |
↓ |
|
| B |
— |
↓ |
↑ |
|
| C |
↓ |
↓ |
||
| D |
↓ |
↑ |
根据上述实验现象,则A、B、C、D四瓶溶液的溶质分别是(用化学式表示):、、、。
标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂和还原剂
(1) Fe2O3+3Al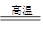 Al2O3+3Fe
Al2O3+3Fe
氧化剂是,还原剂是
(2)2KMnO4+ 16HCl(浓) ="==" 2KCl+ 2MnCl2+ 5Cl2↑ + 8H2O
氧化剂是,还原剂是
按要求填空:
(1)0.2molO3和0.3molO2的质量(选填“相等”、“不相等”或“无法判断”),分子数之比为,所含原子数之比为,在相同条件下的体积之比为。
(2)73g HCl气体中含有个分子,标准状况下占有的体积为L。
(3)相同物质的量浓度的KCl、CuCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3︰2︰1时,三种溶液的体积比为。
(4)标准状况下V L氯化氢气体溶解在1L水中,所得溶液的密度为ρg/mL,溶液中溶质的质量分数为ω,物质的量浓度为c mol/L,则ω=(任写一种表达式)。
按要求填空:
(1)除去NaHCO3溶液中的少量Na2CO3的离子方程式为:。
(2)呼吸面具中发生反应的化学方程式为:。
(3)由铝盐制取氢氧化铝的离子方程式为:。
(4)白色的Fe(OH)2在空气中发生的颜色变化为。
(5)将饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体的化学方程式为:。
有机物A的结构简式为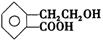 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)指出反应的类型:A→C:。
(2)在A~E五种物质中,互为同分异构体的是(填代号)。
(3)写出由A生成B的化学方程式
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是(填序号)。
(5)C能形成高聚物,该高聚物的结构简为。
(6)写出D与NaOH溶液共热反应的化学方程式
。