已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、SO32-。将这四种溶液分别标记为A、B、C、D,进行如下实验。
①在A或D中滴入C,均有沉淀生成;
②D和B反应生成的气体能被A吸收;
③A和D反应生成的气体能被B吸收,也可使溴水褪色。
试回答下列问题:
(1)D的化学式是________,判断理由是___________________________________________。
(2)写出其余几种物质的化学式:A________,B________,C________。
(3)写出实验②中有关反应的离子方程式_______________________________。
(4)写出③中生成的气体与溴水反应的离子方程式_______________________。
氧氮杂是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质。下面是某研究小组提出的一种氧氮杂化合物H的合成路线: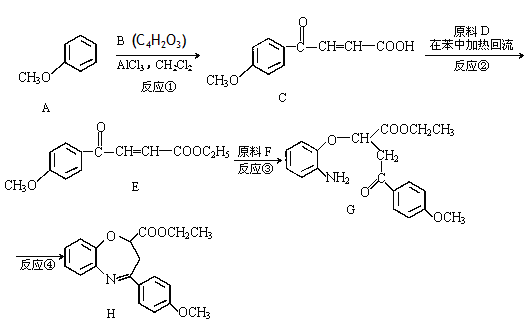
完成下列填空:
(1)写出五元环B的结构简式: 。
(2)有机物E中含有的含氧官能团名称是________、__________和酯基;反应③的反应类型是_____________。
(3)写出符合下列条件的C的一种同分异构体的结构简式: 。
①能发生水解反应且产物之一能发生银镜反应;
②与氯化铁溶液发生显色反应;
③含有四种不同化学环境的氢;
④只含有一个环,且苯环无氢原子。
(4)写出反应②的化学方程式
______________________________________________。
(5)已知:①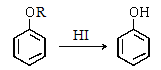 (R为烃基)
(R为烃基)
②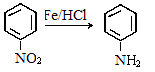
③酚具有还原性,能被氧化剂氧化。
写出以A和丙烯醛(CH2=CHCHO)为原料制备的合成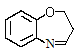 路线流程图(无机试剂任用)。合成路线流程图示例如下:
路线流程图(无机试剂任用)。合成路线流程图示例如下: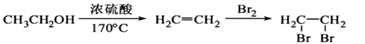
(12分)工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下: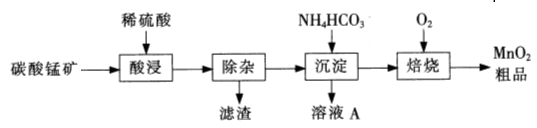
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Pb(OH)2 |
Mn(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
8.0 |
8.3 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
8.8 |
9.8 |
请问答下列问题:
(1)为了提高锰矿中锰元素的浸取率,可采取的措施为 。
(2)写出焙烧过程反应的化学方程式 。
(3)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应离子方程式:
。
(4)某兴趣小组在实验室中除去酸浸后的溶液有少量Fe2+、Fe3+.A13+、Pb2+等,得到只含的Mn2+、 SO42-的溶液,其除杂过程设计如下: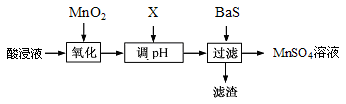
①加入MnO2氧化时发生的离子方程式为 。
②试剂X最好选用 (填字母)。
a.NaOH 溶液 b。KMnO4溶液 c。稀硝酸 d.MnCO3
③滤渣的成分是 。
感光性高分子也称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料,其结构简式为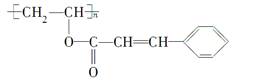
试回答下列问题:
(1)若它是由两种单体经酯化后聚合而成的,试推断这两种单体的结构简式
________________________、______________________
(2)写出在(1)中由两种单体生成高聚物的各步化学反应方程式:
________________,____________________________________。
(3)对此高聚物的性质判断正确的是________
| A.在酸性条件下可以发生水解 |
| B.此高聚物不能使溴水褪色 |
| C.此高聚物可以使酸性高锰酸钾溶液褪色 |
| D.此高聚物水解后可得到另外一种高聚物 |
PMAA是一种“智能型”大分子,可用于生物制药中大分子与小分子的分离,而有机玻璃(聚甲基丙烯酸甲酯)可作飞机、汽车等的窗玻璃、防弹玻璃。下列是以物质A为起始反应物合成PMAA和有机玻璃的路线: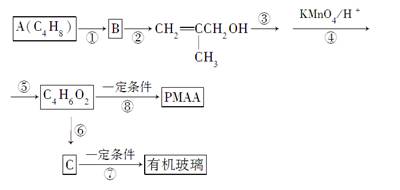
完成下列填空:
(1)写出结构简式:A____________,B____________,PMAA______________。
(2)写出反应类型:反应①________;反应③______;反应⑥________。
(3)写出反应条件:反应②________,反应⑤______________________。
(4)反应③和⑤的目的是_________________________________。
(5)写出反应⑦的化学方程式______________________________。
科学家通过乙二醇的桥梁作用把阿司匹林连接在高聚物上,制成缓释长效阿司匹林,用于关节炎和冠心病的辅助治疗,缓释长效阿司匹林的结构简式如下: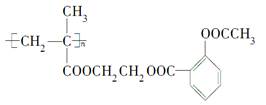
试填写以下空白:
(1)高分子载体结构简式为________。
(2)阿司匹林连接在高分子载体上的有机反应类型是________________。
(3)缓释长效阿司匹林在肠胃中变为阿司匹林的化学方程式是______________________。