铁是生产、生活中应用最广泛的一种金属。以下是初中化学中有关铁的性质的一些基本实验: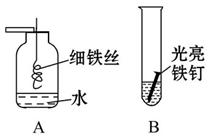
(1)某同学用向上排空气法收集一瓶氧气做A实验,在引燃的火柴快燃尽时将细铁丝插入集气瓶中,未观察到剧烈燃烧,火星四射现象,其原因可能是_________________________________________(写出一条)。
若B中为稀盐酸,观察到的现象是____________________________________;
若B中为硝酸银溶液,反应的化学方程式为____________________________;
若B中为水,一段时间后,产物主要成分的化学式为____________________。
(2)通过以上实验你得出的结论是____________________。
将一定量的锌粉投入到硝酸银、硝酸铜和硝酸镁的混合溶液中,充分反应后过滤,得到滤液和滤渣,写出一定发生的反应方程式 ;若所得滤液呈无色,则滤液中一定含有的金属阳离子为 (填离子符号)滤渣中可能含有的金属单质为 。
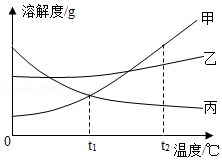
甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题
(1)三种物质中 的溶解度随温度变化趋势与气体溶解度的变化相似(填“甲”或“乙”或“丙”)
(2)将t2℃时甲,乙两物质饱和溶液分别蒸发等质量的水,析出固体的质量甲 乙(填“>”或“<”或“=”)
(3)当甲中混有少量乙时,可采用 的方法提纯甲
(4)将t2℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为 。
端午节到了,学校组织学生到郊外踏青,请用化学知识回答下列问题:
(1)同学们刚下车就闻到阵阵花香,这是因为 (从微观角度回答);
(2)妈妈给小明带了用糯米和火腿瘦肉制作的肉粽,它能为人体提供的两种主要营养素是 。
肉粽被保存在密封的型料包装袋中,该塑料制品应具有 (填“热塑性”或“热固性”)。
(3)同学们在树林里发现了马蜂窝,老师劝诫别干”插马蜂窝”的傻事,因为马蜂体内含有一种碱性物质,蛰咬后疼痛难忍,若发生此事故,就医前可用厨房中的 (填调味品)先做简单处理,缓解疼痛;
(4)返回时老师提醒同学们要把矿泉水瓶等垃圾随身带走,这个行为有利于缓解 (填一种环境问题);绿水青山是我们宝贵的资源,请针对防治水体污染给出一条合理化建议 。
用化学用语表示
(1)铵根离子 ;
(2)保持汞化学性质的最小粒子 ;
(3)实验室中常用的燃料 ;
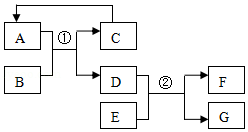
已知A~G均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C能参与植物光合作用;B为赤铁矿主要成分;F是紫红色金属。根据如图所示的转化关系(图中反应条件均已略去),请回答:
(1)写出E的化学式 ;
(2)写出①对应的化学反应方程式 ;
(3)写出②对应的基本反应类型 。