某化学小组参观制碱厂后,绘制了该厂生产纯碱的工艺流程图如下,据图回答:
(1)流程Ⅰ是依次向粗盐水中加入Ca(OH)2和Na2CO3,二者加入的顺序能否颠倒?为什么? 。
(2)用一个化学反应方程式表示出流程Ⅱ中发生的总反应 。
(3)如果不将氯化铵作为目标产品,即加入氨气不是为了生产出氯化铵,那么,氨气在制碱过程中的作用是 。
(4)工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是 。
某兴趣小组的同学发现,上个月做实验用的氢氧化钠溶液忘记了塞上瓶塞。这瓶溶液有没有变质呢?同学们想一探究竟,请你和他们一起参与。
【查阅资料】氯化钡溶液显中性。
【提出猜想】假设一:该溶液没有变质;
假设二:该溶液部分变质;
假设三:该溶液变质。
【实验验证】
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量该溶液于试管中,向其中滴加过量的氯化钡溶液; |
生成白色沉淀 |
假设不成立 |
| ②静置,向上层清液中滴加酚酞溶液。 |
溶液 |
假设二成立 |
【讨论交流】
(1)步骤①滴加过量的氯化钡溶液的目的是;
(2)有同学提出用氢氧化钡溶液代替氯化钡溶液做同样的实验,也能看到相同的现象,得出相同的结论。你同意他的观点吗?为什么?
,。
【反思】氢氧化钠敞口放置变质的原因是(用化学方程式表示),因此氢氧化钠应保存。
【定量研究】
从该瓶中取出一定量的溶液,向其中加入含7.4g氢氧化钙的石灰水,恰好完全反应,过滤,将滤液蒸干,得到12g白色固体。则所取的溶液中含碳酸钠和氢氧化钠的质量分别是多少克?
某同学取一块表面完全锈蚀的生铁片进行了以下探究:
(1)实验: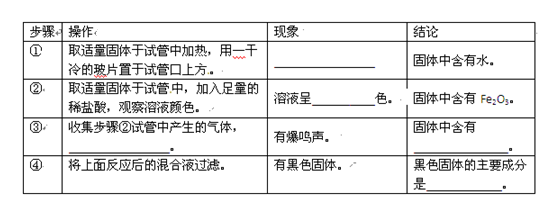
(2)表达:步骤②的化学方程式为__________________、___________________。
(3)拓展:取2枚未生锈的铁钉,一枚部分浸入蒸馏水、另一枚部分浸入盐水,生锈较快的是______________。
现有以下装置、仪器和药品。请根据要求回答问题: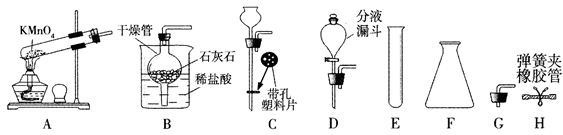

(1)写出仪器的名称: E__________、F__________。
(2)图A的实验室制氧气装置有两处错误,请改正错误____________;___________。
(3)装置B中反应的化学方程式为_______________________________;
(4)把H与B组合,操作弹簧夹可以使反应停止或发生,还可以在“C至H”中选择仪器_______(填序号)组装一个可随时使反应发生或停止的装置;若用H2O2和MnO2制取O2,且能获得平稳的气流,应选E(或F)和______组合。
(5)若用图Ⅰ所示医用塑料袋排空气法收集H2,则H2导入端为_________(填“a”或“b”)。
(6)用图J所示矿泉水瓶可以证明CO2能溶于水且能与水反应的现象是______、
实验室常用下列装置来制取氧气:
(1)写出图中有标号仪器的名称:a、b;
(2)用过氧化氢溶液和二氧化锰来制取氧气时,可选用的发生装置是(填序号);
(3)用E装置收集氧气的依据是
检验氧气是否集满的方法是
(4)写出一个实验室制取氧气的文字表达式为
该反应属于哪种基本反应类型;
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小。氨气极易溶于水。制取并收集氨气,应该从上图中选择的发生装置是,收集装置是______;
(6)一氧化氮气体密度比空气大,常温下会与氧气反应生成二氧化氮,一氧化氮气体不易溶于水。则收集一氧化氮气体的装置是
(7)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管(填“a”或“b”)端连接在供氧气的钢瓶上。
有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题。
(1)A处在给氧化铁加热时温度不够高如何改进?
写出A处改进后发生反应的化学方程式
(2)在C处看到的现象是说明反应后有生成,反应的化学方程式为。
(3)本实验设计中,在B处所采取措施的目的是,
其优点是。