在制玻璃的原料中,再加入下列物质后,可制得各种不同用途的玻璃:
| A.氧化亚铜(Cu2O) | B.氧化钴(Co2O3) |
| C.氧化铅(PbO) | D.硼砂(Na2B4O7·10H2O) |
(1)制造化学仪器的玻璃需加入的物质是______。
(2)制造光学仪器的玻璃需加入的物质是______。
(3)制造蓝色玻璃需加入的物质是____________。
(4)制造红色玻璃需加入的物质是____________。
、高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子,制取高铁酸钠的化学方程式如下:
2Fe(NO3)3+16NaOH+3Cl2 = 2Na2FeO4+6NaNO3+6NaCl+8H2O
(1)标出该反应中电子转移的方向和数目。
(2)在上述反应中 (填元素名称)元素被氧化,氧化剂是 (填化学式)。
(3)当有2.408×1024 个电子发生转移时,参加反应的氯气在标准状况下的体积为 。
(4)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂。在水处理过程中,Na2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体中分散质粒子直径的范围是 ,向Fe(OH)3胶体中逐滴加入HCl稀溶液至过量,会出现的现象是: .
(1)下列物质能导电的是 ,属于电解质的是 。
①NaOH固体 ②液态SO2 ③液态醋酸 ④液态金属钠
⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧融化的KNO3
(2)按要求写出下列方程式:
①钠与水反应的离子方程式:
②将NaHSO4溶液逐滴加入到Ba(OH)2溶液中,当Ba2+恰好沉淀完全时的离子方程式为:
(3)根据离子方程式,写出一个符合条件的化学方程式
CaO+2H+=Ca2++H2O
(4)今有K2SO4和Al2(SO4)3的混合溶液,其中K+物质的量浓度是0.2mol·L-1,SO42-物质的量浓度是0.7mol·L-1。则混合溶液中Al3+物质的量浓度应等于
下面有几种物质,请按要求回答问题。
①食盐与沙子
②从NaCl溶液中获得晶体
③水和汽油的混合物
④用CCl4提取碘水中的碘
(1)分离①、②的操作分别为___________、___________。
(2)③和④共同使用的仪器且在其他组分分离时无需使用,这种仪器是_______。
(3)上述需使用酒精灯的是________(填序号)。
(4)从碘的四氯化碳溶液中得到纯净的碘的方法是 。
已知反应:①SO3+H2O====H2SO4 ②Cl2+H2O====HCl+HClO
③2F2+2H2O====4HF+O2↑ ④2Na+2H2O====2NaOH+H2↑
⑤2Na2O2+2H2O====4NaOH+O2↑ ⑥SiO2+2NaOH====Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有__________(填序号,下同)。H2O被氧化的是___________,H2O被还原的是____________。属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的有_____________。
(2)写出方程式②的离子方程式_____________。
(3)用双线桥标出方程式④中电子转移的方向和数目_______________。
质子交换膜燃料电池广受关注.
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气.
已知:C(s)+1/2O2(g)═CO(g) △H1=﹣110.35kJ·mol﹣1
2H2O(l)═2H2(g)+O2(g) △H2=+571.6kJ·mol﹣1
H2O(l)═H2O(g) △H3=+44.0kJ·mol﹣1
则C(s)+H2O(g)═CO(g)+H2(g) △H4= .
(2)燃料气(流速为1800mL·h﹣1;体积分数为50% H2,0.98% CO,1.64% O2,47.38% N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除.
①160℃、CuO/CeO2作催化剂时,CO优先氧化反应的化学方程式为 .
②灼烧草酸铈[Ce2(C2O4)3]制得CeO2的化学方程式为 .
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度变化如图1所示.加入 (填酸的化学式)的CuO/CeO2催化剂催化性能最好.催化剂为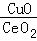 - HIO3,120℃时,反应1h后CO的体积为 mL.
- HIO3,120℃时,反应1h后CO的体积为 mL.
(3)图2为甲酸质子交换膜燃料电池的结构示意图.该装置中 (填“a”或“b”)为电池的负极,负极的电极反应式为