短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说中正确的是( )
| A.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| B.上述四种元素的原子半径大小为W<X<Y<Z |
| C.有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
| D.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 |
A |
B |
C |
D |
E |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的沸点为H2E<H2D B.单质与稀盐酸反应的速率为A<C
C.B与E形成的化合物具有两性 D.A2+与D2-的核外电子数相等
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,如图所示,该装置在工作时,下列叙述正确的是( )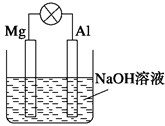
| A.镁比铝活泼,镁失去电子被氧化成Mg2+ |
| B.铝是电池负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.该装置开始工作时,铝片表面的氧化膜不必处理 |
近年来,我国部分地区陆续发现了“毒油”。所谓“毒油”是指混有汽油的食用油,不能食用。下列说法中正确的是( )
| A.汽油是纯净物,有固定的沸点 |
| B.汽油只能由石油分馏得到 |
| C.可用静置后看是否分层来判断食用油中是否混有汽油 |
| D.汽油是含碳原子数为5~11的多种烃的混合物 |
下列各组中的性质比较,正确的是( )
| A.酸性HClO4>HBrO4>HIO4 | B.碱性NaOH>Mg(OH)2>Ca(OH)2 |
| C.稳定性:HI>H2S> HCl | D.氧化性:Na+>Mg2+>Al3+ |