2013年底,上海青浦发生一家三口误食亚硝酸盐造成两男孩身亡的惨剧。常见的亚硝酸盐主要是亚硝酸钠(NaNO2),它是一种白色不透明晶体,虽然形状很像食盐,而且有咸味,但有毒。亚硝酸钠和氯化钠的部分资料如下表:
| |
亚硝酸钠(NaNO2) |
氯化钠(NaCl) |
| 水溶性 |
易溶,溶液呈弱碱性 |
易溶,溶液呈中性 |
| 熔点 |
271℃ |
801℃ |
| 沸点 |
320℃会分解 |
1413℃ |
| 跟稀盐酸作用 |
有红棕色的NO2气体放出 |
无反应 |
完成下列填空:
(1)氮元素最外层电子排布式为________,氮原子核外电子共占据了___个轨道。亚硝酸钠中各元素原子半径由大到小依次为_________,亚硝酸的电离方程式为:_______________________。
(2)亚硝酸盐中毒是因为亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,即血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象.美蓝是亚硝酸盐中毒后的有效解毒剂.下列说法不正确的是( )
A.高铁血红蛋白的还原性比亚硝酸盐弱
B.药品美蓝应具有还原性
C.中毒时亚硝酸盐发生还原反应
D.解毒时高铁血红蛋白被还原
(3)NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须处理后才能排放。处理方法之一:在酸性条件下, NaNO2与KI的物质的量为1:1时恰好完全反应,且I-被氧化为I2,此时产物中含氮的物质(A)为________(填化学式)。若利用上述方法制A,现有两种操作步骤:①先将废水酸化后再加KI;②先将KI酸化后再加入废水。哪种方法较好?____(填序号。假设废水中其它物质不反应)
(4)如要鉴别亚硝酸钠和氯化钠固体,下列方法不可行的是
A.观察并比较它们在水中的溶解速度 B.测定它们各自的熔点
C.在它们的水溶液中滴加甲基橙 D.在酸性条件下加入KI淀粉试液
碳是形成化合物种类最多的元素。
(1)CH2=CH-C≡N是制备腈纶的原料,其分子中 键和
键和 键的个数之比为__________(填最简整数比);
键的个数之比为__________(填最简整数比);
(2)乙醇CH3CH2OH与甲醚CH3OCH3的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是____________________;
(3)某元素位于第4周期VII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_______________.
(6分)下图是某化学兴趣小组同学模拟石蜡油(液态烷烃混合物)深加工来合成CH2=CHCOOCH2CH3(丙烯酸乙酯)等物质的过程:
请回答下列问题:
(1)A的结构简式为_________________;(2)B中所含官能团的名称是___________________;
(3)写出下列反应的化学方程式:
①B+丙烯酸 丙烯酸乙酯___________②苯
丙烯酸乙酯___________②苯 硝基苯____________________
硝基苯____________________
(10分)海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是_____________(填序号);
| A.Cl2 | B.淡水 | C.烧碱 | D.粗盐 |
(2)下图是从海水中提取镁的简单流程。
工业上常用于沉淀 Mg2+的试剂A的名称是__________,,Mg(OH)2转化为MgCl2离子方程是_________海水经蒸发浓缩析出NaCl晶体后的溶液成为卤水,卤水中含有NaBr等无机盐,某实验小组同学设计如下实验流程,模拟工业上从卤水提取工业溴。
①操作I中所涉及到的离子反应方程式为____________.
操作II中所涉及到的化学反应方程式为____________.
②操作II用SO2水溶液吸收Br2,吸收率可达95%,由此反应可知,除环境保护外,在工业生产中还应解决的主要问题是_____________.
③实验小组的同学通过实验发现,如果用未经浓缩的海水直接与Cl2反应,生成的Br2的量会大幅度降低,请你根据所学知识分析原因:_______________________________________.
砷(As)广泛分布与自然界,砷与氮同主族,比氮多两个电子层。
(1)砷位于元素周期表中_____周期________族,其气态氢化物的稳定性比NH3_______(填“强”或“弱”);
(2)砷的常见酸性氧化物有As2O3和As2O5,请根据图中信息写出As2O3分解为As2O5的热化学方程式:________________________;
(3)已知:将酸滴入砷酸盐与KI混合的溶液中发生反应:AsO43-+2I―+2H+=AsO33-+I2+H2O.某研究性学习小组同学欲利用该反应原理,设计实验装置探究原电池原理,请你配合他们绘制原电池装置图,并回答下列问题:
若以石墨为电极,正极上发生的反应为______________.该电池工作时,当外电路中转移5mol电子时,则有_________molI2生成.
工业制氢气的一个重要反应是:CO(g)+H2O(g)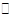 CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知在25。C时:
①C(石墨)+1/2O2(g)=CO(g)△H1=-111kJ·mol-1
②C(石墨)+O2(g)=CO2(g)△H2=-394kJ·mol-1
③H2(g)+1/2O2(g)=H2O(g)△H3=-242kJ·mol-1
则反应CO(g)+H2O(g) ="==" CO2(g)+H2(g)的反应热△H=___________.
(2)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据: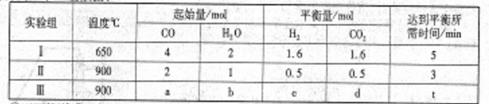
①以下反应能说明CO(g)+H2O(g) CO2(g)+H2(g)达到平衡状态的是_________
CO2(g)+H2(g)达到平衡状态的是_________
| A.容器中CO的含量保持不变 | B.容器中CO2浓度与CO浓度相等 |
C.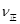 (CO)= (CO)=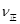 (H2O) (H2O) |
D.容器中混合气体的平均相对分子质量保持不变 |
②实验I中,从反应开始到反应达到平衡时,CO的平均反应速率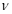 (CO)=_____;
(CO)=_____;
③实验II条件下反应的平衡常数K=_____________(保留小数点后二位);
④实验III中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是______;
⑤若在900℃时,实验II反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时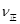 ___________
___________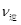 (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
(填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)