已知元素A、B、C、D、E、F均属前四周期且原子序数依次增大,A的p能级电子数是s能级的一半,C的基态原子2p轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。
请回答下列问题。
(1)C原子基态时电子排布式为 。
(2)B、C两种元素第一电离能为 > (用元素符号表示)。试解释其原因: 。
(3)任写一种与AB-离子互为等电子体的离子 。
(4)B与C形成的四原子阴离子的立体构型为 ,其中B原子的杂化类型是 。
(5)F(OH)2难溶于水,易溶于氨水,写出其溶于氨水的离子方程式 。
(6)D和E形成的化合物的晶胞结构如图,其化学式为 ;∠EDE= ;E的配位数是 ;已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶胞边长a= cm。(用ρ、NA的计算式表示)
四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
| 甲 |
乙 |
|
| 丙 |
丁 |
请用化学用语回答:
(1)丙在元素周期表中的位置是___________。
(2)丁单质的电子式是_______________【(2)~(5)用化学用语回答】。
(3)乙的两种常见单质分别是。
(4)甲、丙、丁的气态氢化物水溶液显酸性的是___________。
(5)氢元素与甲和丁可以组成一种既有离子键、又有共价键的化合物,其化学式是。
(6)已知丁的非金属性比丙强,原因是_______________(从原子结构角度解释)。
结晶玫瑰是具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)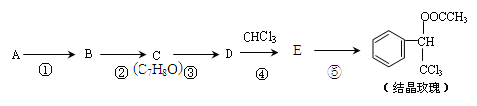
已知:  (-R表示烃基)
(-R表示烃基)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是。
(2)反应②所需药品及反应条件是。
(3)C的核磁共振氢谱峰面积之比是。
(4)⑤的化学方程式是。
(5)C有多种同分异构体,其中属于芳香族化合物的有种。
(13分)X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表:
| 元素 |
结构或性质信息 |
| X |
其原子最外层电子数是内层电子数的2倍 |
| Y |
基态原子最外层电子排布为nsnnpn+1 |
| Z |
非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M |
单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
| Q |
其与X形成的合金为目前用量最多的金属材料 |
(1)Q元素基态原子的电子排布式是:____________。
(2)比较Y元素与氧元素的第一电离能:____>____;X和Z形成的化合物XZ2为一种液体溶剂,其分子中的 键和
键和 键数目之比为:_____。
键数目之比为:_____。
(3)写出实验室制备M单质的离子方程式:_____。
(4)M的气态氢化物和氟化氢相比(写化学式):
稳定性强的是_____________,其原因是_____________________;
沸点高的是_____________,其原因是_____________________。
亚硝酸盐是一种常见的食品添加剂,使用时必须严格控制其用量。为检测某食品中亚硝酸盐含量(通常以1kg样品中含NaNO2的质量计),某研究小组设计了如下两种实验方案:(提示 : 无色气体B遇空气显红棕色)
(1)甲方案②中常用做指示剂。若需配制80 mL0.001 mol·L-1的Na2S2O3标准溶液。现给出下列仪器(配制过程中可能用到):①50 mL烧杯②胶头滴管③天平④80 mL容量瓶⑤100 mL容量瓶⑥玻璃棒,按使用仪器的先后顺序排列正确的是
| A.③①⑤⑥② | B.③①⑥④② | C.③①⑥⑤② | D.③①④⑥② |
请写出配制Na2S2O3标准溶液时定容的操作
(2)已知酸性条件下MnO4—被还原为Mn2+,请写出乙方案①的离子方程式
(3)若取样品ag,按乙方案进行测定,准确量取12.00mL0.0005mol/L的酸性KMnO4溶液(过量)与溶液A反应。反应后溶液用0.0010mol/L(NH4)2Fe(SO4)2标准溶液滴定至溶液紫色刚好褪去;重复上述实验2次,平均消耗(NH4)2Fe(SO4)2溶液10.00mL.则1kg样品中 NaNO2的质量为_______mg.
(4)若乙方案②中使用的(NH4)2Fe(SO4)2溶液暴露在空气中时间过长,则会导致测定出的NaNO2含量(填“偏高”、“偏低”或“不影响”)
(5)小组经过讨论,认为方案更佳,原因是。
SO2、NO是大气污染物。工业上吸收SO2和NO,同时获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):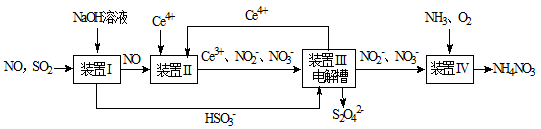
(1)装置Ⅰ中生成HSO3-的离子方程式为;
(2)向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:;
(3)装置Ⅲ中,电解槽的阳极发生的电极反应为;
(4)从装置Ⅳ中获得粗产品NH4NO3的实验操作依次为、、过滤、洗涤等。