有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。
B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。
A.A>B>C>D B.A>B>D>C
C.D>A>B>C D.D>C>A>B
下列变化可以直接通过取代反应来实现的是
A.CH3CH2OH CH3CHO CH3CHO |
B.CH2=CH2 CH3—CH2Br CH3—CH2Br |
C.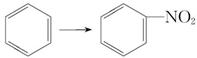 |
D.CH3COOH (CH3COO)2Ca (CH3COO)2Ca |
实验室中,下列除去括号内杂质的有关操作正确的是
| A.苯(硝基苯):加少量蒸馏水振荡,待分层后分液 |
| B.乙醇(水):加新制的生石灰,蒸馏 |
| C.CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 |
| D.乙烷(乙烯):通入氢气发生加成反应 |
下列关于有机化合物的说法正确的是
| A.分子式为C3H6O2的链状有机物中含有一个双键 |
| B.1 mol甲烷与Cl2完全发生取代反应需2 mol Cl2 |
| C.1 mol乙烯与Cl2完全发生加成反应需2 mol Cl2 |
| D.乙醇与乙酸均能被酸性KmnO4溶液氧化 |
下列现象中,是因为发生加成反应而产生的现象是
| A.乙烯使酸性高锰酸钾溶液褪色 |
| B.将苯滴入溴水中,振荡后水层接近无色 |
| C.乙烯使溴的四氯化碳溶液褪色 |
| D.甲烷与氯气混合,光照一段时间后黄绿色消失 |
根据下列事实所作的结论,正确的是
| 编号 |
事实 |
结论 |
| A |
甲、乙两种有机物具有相同相对分子质量和不同结构 |
甲和乙一定是同分异构体 |
| B |
质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 |
甲、乙两种分子中,各元素的原子个数比一定相同 |
| C |
在淀粉液中加入稀H2SO4,水浴加热一段时间后取出部分水解液,滴加新制银氨溶液后再加热,无银镜出现 |
淀粉水解产物不具有还原性 |
| D |
不存在两种邻二甲苯 |
苯分子中碳碳键完全相同,而不是单双键交替结构 |