以下四个实验方案,用以检验淀粉的水解情况。
(1)方案甲:淀粉 水解液
水解液 中和液
中和液 溶液变蓝
溶液变蓝
结论:淀粉完全没有水解
(2)方案乙:淀粉液 水解液
水解液 无砖红色沉淀
无砖红色沉淀
结论:淀粉没有水解。
(3)方案丙:淀粉液 水解液
水解液 中和液
中和液 有砖红色沉淀
有砖红色沉淀
结论:淀粉已水解。
(4)方案丁:
结论:淀粉部分水解
以上四种方案的设计及结论是否正确?如不正确,请简述理由。
常温时,将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为:
| A.1:9 | B.9:1 | C.10:1 | D.1:10 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法不正确的是:
| A.在熔融电解质中,O2-移向负极 |
| B.电池的总反应是:2C4H10+13O2=8CO2+10H2O |
| C.通入空气的一极是正极,电极反应为:O2+4e-=2O2- |
| D.通入丁烷的一极是正极,电极反应为:C4H10+26e-+13O2-=4CO2↑+5H2O |
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
| A.加MgCl2 | B.加H2O | C.加NaOH | D.加HCl |
25 ℃、101 kPa下:①2Na(s)+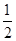 O2(g)===Na2O(s) ΔH1=-414 kJ·mol-1
O2(g)===Na2O(s) ΔH1=-414 kJ·mol-1
②2Na(s)+O2(g)===Na2O2(s) ΔH2=-511 kJ·mol-1
下列说法正确的是
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)===2Na2O(s) ΔH=-317 kJ·mol-1 |
常温下,将100 mL的0.02 mol·L-1的Ba(OH)2溶液和100 mL的0.02 mol·L-1的NaHSO4溶液混合,若忽略溶液体积变化,则混合后的溶液
| A.pH=2 |
| B.pH=12 |
| C.由水电离产生的c(H+)=1.0×10-2mol·L-1 |
| D.溶质的物质的量浓度为0.02mol·L-1 |