已知钾原子的原子结构示意图为:(如图所示)
(1)钾元素的原子序数为:
(2)钾元素的原子在反应中易 (填“得到”或“失去”) 个电子,表现出 性(填“氧化性”或“还原性”)
(3)钾元素的金属性 (填“强”或“弱”)于钠元素的金属性。
在标准状况下有:① 0.3mol氨气②6.02×1022个H2O分子 ③7.3gHCl④ 0.2molCH4。请将序号填在后面横线上,
体积最大的是;密度最大的是;质量最大的是。
用①质子数、②中子数、③电子数、④质量数、⑤同位素填空,
请将序号填在后面横线上。
(1)136C与147N具有相同的,(2)136C与126C具有相同的,
(3)146C与147N具有相同的,(4)157N与147N互为。
(1)右图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。计算:(要求写出简要计算过程)用该浓硫酸配制200mL1mol/L的稀硫酸,用量筒所需量取该浓硫酸的体积是多少mL?
(2)在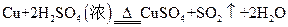 反应中,
反应中,
若有3.2 g的Cu参与反应,则被还原的H2SO4的物质的量是多少?
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若用nA 代表阿伏加德罗常数的数值,则:(只要求写出结果)
(1)该气体的物质的量为________mol。(2)该气体在标准状况下的体积为_________L。
(3)该气体所含原子总数为_______个。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为____。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____mol/L。
欲用36.5%(密度为1.18g/cm3)的浓盐酸配制浓度为1.00mol/L的稀盐酸500mL。

(1)选用的主要玻璃仪器有:①②③④⑤。
(2)现有下列配制操作,正确的操作顺序为:(填字母)
| A.用量筒量取浓盐酸; | B.反复颠倒摇匀; | C.用胶头滴管加水至刻度线; |
| D.洗净所用仪器,洗涤液也转入容量瓶;E.稀释浓盐酸;F.溶液冷却后转入容量瓶。 |
(3)简要回答下列问题:
如果实验室有10mL、50mL、100mL的量筒,应选用mL的量筒。量取时发现量筒不干净,用水洗净后直接量取,将使配制的溶液浓度(填“偏高”、“偏低”或“无影响”)。