硫碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2=H2SO4+2HI
Ⅱ.2HI H2↑+I2
H2↑+I2
Ⅲ.2H2SO4=2SO2+O2↑+2H2O
(1)分析上述反应,下列判断正确的是 。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2的物质的量随时IP间的变化如图所示。
①0~2 min内的平均反应速率v(HI)= 。
②相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.HI的平衡浓度
b.达到平衡的时间
c.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,若加入少量下列固体试剂中的 ,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
已知1g N2含a个分子,则阿伏加德罗常数为。
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下: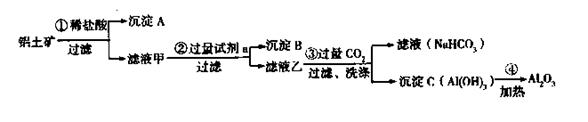
(1)沉淀A、B的成分分别是、;
(2)步骤②中的试剂a是;
(3)试写出步骤③中发生反应的离子方式;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液。在配制250mi。该盐酸溶液时,某同学转移溶液的操作如图所示,图中的主要错误是: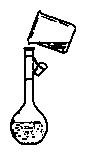
①;
②。
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图所示,则所用盐酸溶液的物质的量浓度为,样品中Al2O3的百分含量为。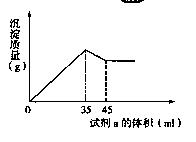
甲、乙、丙是中学中常见的单质,X、Y、Z是常见的化合物。在常温常压下,甲是具有氧化性的黄绿色气体,丙是棕红色的液体,Y与Z含有相同的阳离子,X与Z含有相同的阴离子;它们之间有以下转化关系:丙十乙
→Z;X十丙→Z;X+甲→Y+丙。请回答下列问题:
(1)写出甲、乙、丙三种物质的化学式____、、____;
(2)写出X与足量的甲在溶液中完全反应时的离子方程式。
(3)欲在实验室中制取并收集纯净、干燥的气体甲,然后完成上述反应“X+甲→Y+丙”,某同学设计了如下图所示的装置。
①装置A中发生反应的化学方程式为;
②装置B的作用是;
③装置C中的试剂为;
④装置D中收集气体甲的方法名称是;
⑤装置F的主要作用是,反应原理的离子方程式为。
由Fe2O3、CuO、A1中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):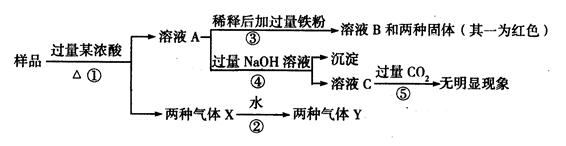
(1)混合气体Y中两种气体的化学式是,反应①中生成混合气体X的化
学方程式是。
(2)通过上述实验及其现象说明,一定不含有的物质是,不能确定是否含有的物质是;
(3)为进一步确定样品中的未知物质,可以用上述反应过程中的溶液,设计一个简单的后续实验就可以确定,方法是。
某无色溶液X,由K+、NH+4、Ba2+、Al3+、Fe3+、CO2-3、SO2-4中的若干种离子组成,取该溶液进行如下实验: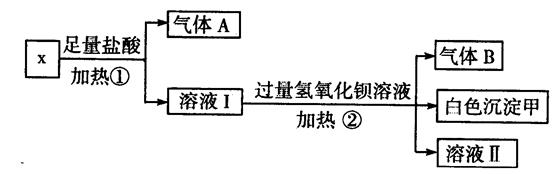
(1)白色沉淀甲是;
(2)试写出实验过程中生成气体A、B的离子方程式、
;
(3)通过上述实验,可确定X溶液中一定存在的离子是,尚未确定是否存在的离子是。