某无色溶液中只可能溶有NH4+、K+、Al3+、Mg2+、HCO3-、Cl-、I-、MnO4-、SO42-等离子中的几种离子。分析其组成,现进行如下实验:
①取l0mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲。
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生。
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0. 03 mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0. 224L(假设丙全部逸出),最后沉淀完全溶解。下列推断正确的是
| A.肯定有K+、Al3+、Mg2+、SO42- |
| B.肯定有K+、NH4+、Al3+、SO42- |
| C.肯定没有K+、HCO3-、MnO4- |
| D.肯定没有K+、NH4+、Cl- |
下列实验操作能达到目的的是
| A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| B.制取二氧化氮时,用水或NaOH溶液吸收尾气 |
| C.为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b g,该方案可行。 |
| D.为测定镀锌铁皮的锌层厚度,将镀锌铁皮与足量盐酸反应待气泡明显减少时取出,洗涤,烘干,称重。若烘干时间过长,会导致测定结果偏小。 |
下列有关阿伏伽德罗常数NA说法错误的是
| A.22 g 2H218O中含有的质子数为10NA |
| B.电解58.5 g熔融的NaCl,能产生11.2 L氯气(标准状况)、23.0 g金属钠 |
| C.1.00 mol NaCl中,所有Na+的最外层电子总数为10NA |
| D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
下列有关操作或说法正确的是
| A.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
| B.金属汞一旦洒落到实验室地面或桌面时,必须尽可能收集,并深埋处理 |
| C.金属钠着火时用泡沫灭火器灭火 |
| D.加工后具有吸水性的植物纤维可用作食品干燥剂 |
下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。请观察如下图所示实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是( )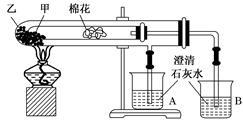
| A.甲为小苏打,乙为纯碱 |
| B.要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 |
| C.加热不久就能看到A烧杯的澄清石灰水变浑浊 |
| D.整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊 |
通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )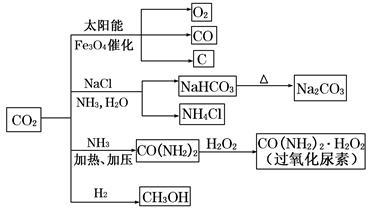
A.CO2经催化分解为C、CO、O2的反应为放热反应
B.除去Na2CO3固体中少量NaHCO3可用热分解的方法
C.过氧化尿素和SO2都能使品红溶液褪色,其原理相同
D.由CO2和H2合成甲醇,原子利用率达100%