下列图示与对应的叙述相符的是
| A.图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.向溶质为1mol的NaOH溶液中通入CO2,随着CO2气体的通入,溶液中水电离出的c(H+)有如上图2变化关系 |
| C.如上图2所示,水电离出c(H+)达到最大值时,溶液中各离子浓度大小分别为 c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)>c(H+) |
| D.用0.0l00mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
一个原电池的总反应的离子方程式是Zn+Cu2+===Zn2++Cu,该原电池的正确组成是
| A |
B |
C |
D |
|
| 正极 |
Zn |
Cu |
Zn |
Fe |
| 负极 |
Cu |
Zn |
A g |
Zn |
| 电解质溶液 |
CuCl2 |
H2SO4 |
CuSO4 |
CuCl2 |
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是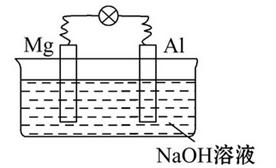
| A.镁比铝活泼,镁失去电子被氧化成Mg2+ |
| B.该装置开始工作时,铝片表面的氧化膜可不必处理 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成 |
铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼胶KNO3的U形管)构成一个原电池,如图: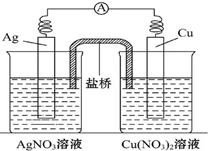
以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-====Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
| A.①② | B.②③ | C.②④ | D.③④ |
下列说法正确的是
| A.构成原电池正极和负极的材料必须是金属 |
| B.在原电池中,电子流出的一极是负极,该电极被还原 |
| C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 |
| D.原电池可以把物质内部的能量全部转化为电能 |
下列说法中正确的是
| A.原电池是把电能转化为化学能的装置 |
| B.原电池中电子流出的一极是正极,发生氧化反应 |
| C.原电池两极均发生氧化还原反应 |
| D.原电池中的阳离子向正极移动 |