2013年10月我市因台风菲特遭受到重大损失,市疾控中心紧急采购消毒药品,以满足灾后需要。复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2是一种无色粘稠液体,请回答下列问题:
(1)下列方程中H2O2所体现的性质与其可以作为消毒剂完全一致的是 。
A.BaO2+2HCl H2O2+BaCl2
H2O2+BaCl2
B.Ag2O+H2O2 =2Ag+O2+H2O
C.2H2O2 2H2O+O2↑
2H2O+O2↑
D.H2O2+NaCrO2+NaOH=Na2CrO4 +H2O
(2)火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g) △H=" -" 534 kJ·mol-1
H2O2(1)=H2O(1)+1/2O2(g) △H=" -" 98.64 kJ·mol-1
H2O(1)=H2O(g) △H=+44kJ·mol-l
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H= ,
该反应的△S= 0(填“>”或“<”)。
(3)H2O2是一种不稳定易分解的物质。
①如图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图
②实验证实,往Na2CO3溶液中加入H2O2也会有气泡产生。已知常温时H2CO3的电离常数分别为Kal=4.3×l0-7,Ka2 =" 5.0" ×l0-11 。Na2CO3溶液中CO32-第一步水解常数表达式Khl= ,常温时Khl的值为 。若在Na2CO3溶液中同时加入少量Na2CO3固体与适当升高溶液温度,则Khl的值
(填变大、变小、不变或不确定)。
(4)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。
注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L-l的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是 (填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小
有机物OPP是用途十分广泛的有机化工产品,广泛应用于杀菌防腐、印染助剂、表面活性剂、稳定剂和阻燃剂等领域。以烃A为原料可合成OPP: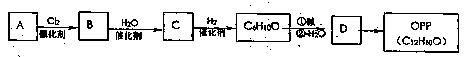
已知醛或酮在碱催化下可发生如下反应: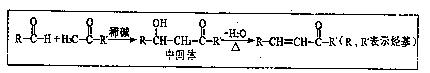
(1)①烃A是无色、带有特殊气味的液体。经实验测定,烃A中碳定元素和氢元素的质量比为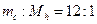 。烃A的结构简式为。
。烃A的结构简式为。
②(填操作名称)是分离、提纯液态有机物的常用方法,烃A就是用该方法从煤焦油中得到的基本化工原料。
(2)烃A生成有机物B的反应类型为。
(3)①有机物C(分子式为C6H6O)能与NaOH反应:
②有机物C与浓溴水反应生成白色沉淀,可用于有机物C的定性检验和定量测定,该反应的化学方程式为。
(4)有机物C6H10O的红外光谱图显示分子中含有C=O键,但是C6H10O不能发生银镜反应。C6H10O的结构简式为。
(5)有机物D的结构简式为。
某学生设计如下实验装置利用氯气与潮湿的消石灰应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
(1)A仪器的名称是,所盛试剂的名称是。B中发生反应的离子方程式是。
(2)漂白粉将在U型管中产生,其化学反应方程式是。
(3)有同学建议在两个橡皮套管内的两段玻璃导管管口应尽量紧靠,原因是。
(4)此实验所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了氯酸钙[Ca(ClO3)2],为避免此副反应的发生,可采取的措施是;
②另一个副反应是:Ca(OH)2+2HCl=CaCl2+2H2O。
为避免此副反应发生,可采取的措施是在B、C之间连接一个盛有的洗气瓶。
A、B、C、D是四种常见的单质,A、B为金属;C、D常温下是气体,且D为黄绿色气体。甲、乙、内为常见的化合物,甲物质具有磁性。它们之间有如图1的转化关系:
请回答下列问题:
(1)B与甲反应的化学方程式是。
(2)含有B的阳离子的溶液与乙溶液反应得到一种白色沉淀,该反应的离子方程式是。
(3)实验室检验丙溶液中所含金属阳离子的操作方法和 现象是。
现象是。
(4)电浮选凝聚法是工业上采用的一种污水处理方法,如图2是该方法处理污水的实验装置示意图,实验过程中,污水的pH始终保持在5.0~6.0之间。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用。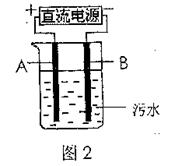
阳极的电极反应分别是,2H2O-4e-=4H++O2↑;
阳极区生成沉淀的离子方程式是。
X、Y、Z为周期表中前20号主族元素,原子序数递增,X、Y原子的最外层电子数 是其电子层数的2倍,Z是人体中含量最高的金属元素。
是其电子层数的2倍,Z是人体中含量最高的金属元素。
(1)下列含氧酸根化学式书写不正确的是(填序号)。
a.XO3- b.XO32- c.YO32-d.Y2O32-
(2)X、Y的原子可构成只含极性键的非极性分子;它的电子式是,空间构型是。
(3)Y的最高价含氧酸是重要的化工产品。
①已知YO2被空气氧化,每生成1mol气态YO3,放出98.3kJ热量。该反应的热化学方程式是。
②实验测得相同条件下一定量的Y单质分别在空气和在氧气中充分燃烧后产物的成分(体积分数)如表。Y在纯氧中燃烧的产物中YO3含量比空气中少,试分析其原因。
| YO2 |
YO3 |
|
| 空气 |
94%—95% |
5%—6% |
| 氧气 |
97%—98% |
2%—3% |
2,3-二氢呋喃是抗肿瘤药物的中间体,也用于电子化学品和香料中,可由丙烯为原料合成: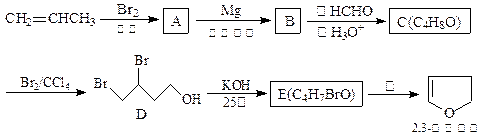
已知:
1、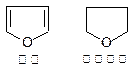
2、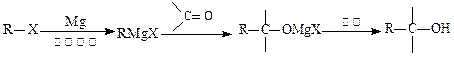
回答下列问题:
(1)请用系统命名法命名化合物D。
(2)①反应③的条件是。
②写出C、E的结构简式:
C、E。
(3)工业上由化合物F(C4H10O2)在少量硫酸存在下可制得四氢呋喃,写出反应方程式: 。
。
(4)写出满足下列条件的呋喃的一种同分异构体的结构简式。
① 没有支链,且一取代产物只有两种;
② 与银氨溶液不发生银镜反应。
(5)2,3-二氢呋喃在一定条件下可以转变成四氢呋喃,如何用简单的化学方法检验2,3-二氢呋喃是否完全转化?