下表中对离子方程式的评价不合理的是
| 选项 |
化学反应及离子方程式 |
评价 |
| A |
NaClO溶液中通入少量的SO2:ClO-+H2O+SO2===Cl-+SO42-+2H+ |
错误,碱性介质中不可能生成H+ |
| B |
用酸性高锰酸钾溶液滴定草酸:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O |
正确 |
| C |
NH4Al(SO4)2溶液中滴入几滴NaOH溶液:NH4++OH-===NH3·H2O |
错误,OH-首先和Al3+反应生成Al(OH)3沉淀 |
| D |
用惰性电极电解MgCl2溶液:2Mg2++2H2O 2Mg+O2↑+4H+ 2Mg+O2↑+4H+ |
正确 |
某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4===3N2+4H2O,反应温度可达2 700 ℃,对于该反应,下列说法正确的是
| A.该反应属于置换反应 |
| B.N2H4是氧化剂 |
| C.N2O4发生氧化反应 |
| D.氧化产物与还原产物的质量比为2:1 |
下列说法正确的是
| A.需要加热的化学反应都是吸热反应 |
| B.水力发电是将化学能转化为电能的过程 |
| C.某吸热反应能自发进行,因此该反应是熵增反应 |
| D.原电池是将电能转化为化学能的一种装置 |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如下图装置①。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列叙述不正确的是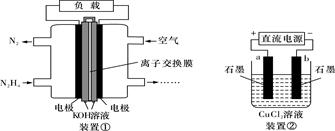
| A.该燃料电池负极发生的电极反应为:N2H4+4OH--4e-===N2+4H2O |
| B.用该燃料电池作为装置②的直流电源,产生1 mol Cl2至少需要通入0.5 mol N2H4 |
| C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D.该燃料电池中,电子从右侧电极经过外电路流向左侧电极,溶液中OH-则迁移到左侧 |
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,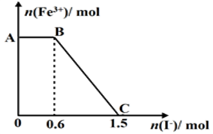
下列说法中不正确的是
| A.图中AB段的氧化剂为K2Cr2O7 |
| B.图中BC段发生的反应为2Fe3++2I- =2Fe2++I2 |
| C.开始加入的K2Cr2O7为0.25 mol |
| D.K2Cr2O7可与FeSO4反应的物质的量为1:3。 |
A、B、C、D、E五种短周期元素原子序数依次增大,A原子为半径最小的原子,C原子最外层电子数与A、B原子最外层电子数之和相等,D原子和B原子最外层电子数的和为C原子最外层电子数的2倍,D原子的最外层电子数为电子层数的3倍,A、E同一主族。下列说法正确的是
A.原子半径大小顺序为:E>D>C>B>A
B.A、B、C、D四种元素都属于非金属元素,它们之间只能形成共价化合物
C.B、C、D、E四种元素与A 元素形成的最简单化合物的沸点依次升高
D.D与A、E均可形成具有强氧化性的化合物,可用于城市自来水的杀菌消毒