在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是 、 。
(2)取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是 。
(3)在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL。
(4)将不纯的NaOH样品1 g(样品含少量Na2CO3和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到 克固体。
(本题共10分)有机物(C6H12)的两种异构体A和B和其他一些有机物之间有如图所示的转化关系。其中G的一氯取代物只有两种,A的分子结构中有3个甲基,B转变为F时只有一种产物。
请填写下列空白:
48、上述转化过程中,属于加成反应的是____________(填序号)。
49、有机物G的名称为_________________________。
50、有机物A和C12H22O3结构简式分别为:A_________________、C12H22O3_________________。
51、写出②、③、两步反应的化学方程式:
②_______________________________________________________________________;
③_______________________________________________________________________。
52、A在一定条件下发生加聚反应的化学方程式:__________________________________。
(本题共12分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下: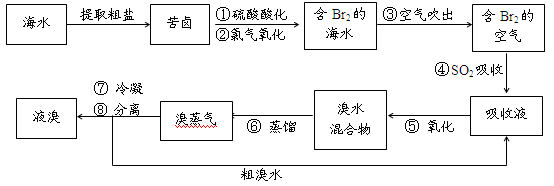
41、溴在元素周期表中位于_________周期,_________族。
42、步骤①中用硫酸酸化可提高Cl2的利用率,其原因是。
43、步骤④的离子方程式:_______________________________________。
44、步骤⑥的蒸馏过程中,溴出口温度要控制在80—90℃。温度过高或过低都不利于生产,请解释原因:__________________________________________。
45、步骤⑧中溴气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是_____________,分离时液溴从分离器的_____(填“上口”或“下口”)排出。
46、不直接用步骤②后含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氧化”的原因是。
47、下列有关溴单质的叙述正确的是
| A.是易挥发的深红棕色液体 |
| B.实验室少量液溴可保存在橡皮塞的棕色瓶中,并且加少量的水液封 |
| C.可用酒精从溴水中萃取溴 |
| D.溴可以与NaI溶液反应,置换出碘单质 |
(本题共12分)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
36、在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发、_________、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________。
a. 蒸发的目的是得到热饱和溶液
b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液
d. 应蒸发至有较多晶体析出时为止
37、由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________。
a. 得到热饱和溶液b. 析出晶体
38、若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:___________________;用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_______________________________________________________________。
39、该流程产生的物质中,除Ca2+能被海洋生物利用外,还需综合利用的物质是_________。
40、MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和水,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a:b≈______________(取整数值)。
(本题共11分)本题有2小题。在一体积为2L的密闭容器中,气态物质A、B、E的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度A的转化率增大。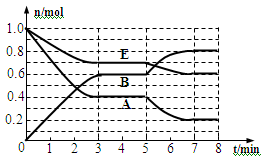
29、写出此反应的化学方程式_________________________________;此反应是___________热反应。
30、根据图数据,从反应开始到第一次达到平衡时平均速率v (E)为________________。
31、在5~7 min内曲线变化的原因可能是____(填编号)
A. 降低了温度 B. 使用了催化剂
C. 减小了容器的体积 D. 减少了A的物质的量
32、设该反应达到平衡时的平衡常数为K1,保持温度不变,将容器体积减少一半,达到新的平衡后,测得B的平衡浓度为原来的2.2倍,平衡常数为K2,则_______(填编号)
A. 平衡向正反应方向移动,且K2 > K1
B. 平衡移动过程中,正反应速率大于逆反应速率
C. 达到新平衡时,A的浓度增大,且K1 > K2
D. 达到新平衡时,E的浓度是原来的2倍多,且K1 = K2
已知在25℃时,亚硝酸、次氯酸和氢硫酸的电离常数分别为:
亚硝酸 Ki = 4.6×10-4
次氯酸 Ki = 3.0×10-8
氢硫酸 Ki 1= 9.1×10-8Ki 2 = 1.1×10-12
33、写出氢硫酸的第一级电离平衡常数表达式:Ki1 = _________________。
34、在相同条件下,试比较H2S、HS-、HClO和HNO2的酸性强弱:______>______>_____>_______。
35、保持温度不变,在氢硫酸溶液中加入少量盐酸,下列量会变小的是_____(填序号)
A.c(S2-)
B.c(H+)
C.Kw
D.氢硫酸电离平衡常数
E.氢硫酸的电离度
(本题共13分)A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E顺序增大;C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A和气体物质EB4;EB4蒸气的密度是相同条件下空气密度的3.586倍。
23、指出A在元素周期表中的位置_________。
24、写出D2A2的电子式__________;写出CB与EA2反应的化学方程式___________________。
25、下表是不同物质中的键长和键能的数据,其中a、b、d未知,通过表中的数据分析,估计出a、b、c、d的大小顺序为______________________________。
| 共价键 |
C-C |
C=C |
 C C C C |
C-O |
C=O |
H-F |
N=N |
 N N N N |
| 键长(nm) |
0.154 |
0.134 |
0.120 |
0.143 |
0.122 |
0.092 |
0.120 |
0.110 |
| 键能(kJ/mol) |
a |
b |
358 |
c=805 |
569 |
d |
氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
26、不能通过电解纯净的液态HF获得F2,其原因是_________;但电解液态KHF2时,两极分别得到F2和H2,则F2在电解池的_____极产生。
27、利用化学反应也能制取氟。请配平下列化学方程式:
____K2MnF6+____SbF5→____KSbF6+____MnF3+____F2↑
28、一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随pH的分布曲线如图示。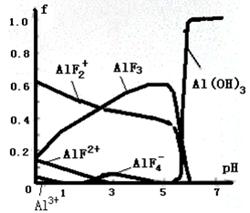
用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式:____________________。