近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式: 。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式: 。
③写出步骤(Ⅲ)反应的离子方程式: 。
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42-的转化率。
①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是 。(填写序号)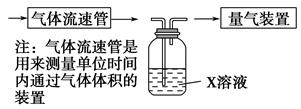
| A.碘的淀粉溶液 | B.酸性高锰酸钾溶液 |
| C.氢氧化钠溶液 | D.氯化钡溶液 |
②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO 的转化率,已知气体流速,还需测定的数据有 、 。
的转化率,已知气体流速,还需测定的数据有 、 。
A、B、C三种有机物,其相对分子质量都小于150,已知B完全燃烧时所消耗的O2和生成的CO2的物质的量相等,C中碳、氢元素总的质量分数为48.39 %。在热的稀硫酸溶液中,1 mol A水解能生成2 mol B和1 mol C。B不能发生银镜反应,但能与NaHCO3溶液反应放出CO2。回答下列问题:
(1)B的分子组成中氢氧原子个数比为;
(2)有机物C的结构简式为;
(3)有机物A的结构简式为;
(4)写出有机物A水解生成B和C的化学方程式。
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。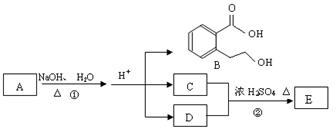
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为; C分子中的官能团名称是 ______________;化合物B不能发生的反应是(填字母序号):
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.置换反应
(2)反应②的化学方程式是__________________。
(3)A的结构简式是 __________________。
(4)同时符合下列三个条件的B的同分异构体的数目有个。
Ⅰ.含有间二取代苯环结构
Ⅱ.不属于芳香酸形成的酯
Ⅲ.与 FeCl3溶液发生显色反应。
写出其中任意两个同分异构体的结构简式、。
芳香族化合物C10H10O2有如下的转化关系: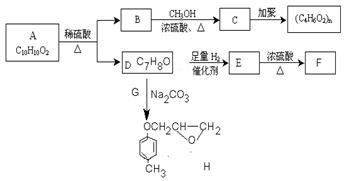
已知F能使Br2/CCl4溶液褪色,且RONa + R’X→ROR’ + NaX
请回答下列问题:
1.写出反应类型。
反应B → C反应 E→F
2.请分别写出A、F的结构简式
AF
3.若有机物M与C互为同分异构体,
则与有机物B互为同系物的M的同分异构体有种。
4. 请写出B→C反应的化学反应方程式
5.请写出D→H反应的化学反应方程式
提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| 括号内为杂质 |
除杂试剂 |
操作 |
|
| 1 |
乙炔(硫化氢) |
||
| 2 |
溴苯(溴) |
||
| 3 |
硬脂酸钠(甘油) |
||
| 4 |
乙醇(水) |
已知:①具有一个甲基支链的化合物A的分子式为C4H6O2,A可以使Br2的四氯化碳溶液褪色,1molA和1mol NaHCO3能完全反应。②化合物B含有C、H、O三种元素,相对分子质量为60,其中碳的质量分数为60%,氢的质量分数为13.3% 。B在催化剂Cu的作用下被氧气氧化成C,C能发生银镜反应。③A和B在浓硫酸加热条件下可生成有水果香味的D。回答下列问题:
(1)写出A的结构简式:________________________
(2)C名称为__________________
(3)写出B的结构简式:___________________________