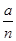W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
| W |
X |
|
| |
Y |
Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性强于Y
D.Z元素单质在化学反应中只表现氧化性
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是()
CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是()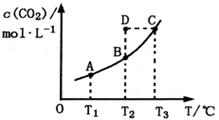
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH>0 CO2(g)+H2(g)的ΔH>0 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
| D.恒压密闭容器中通入1mol CO(g)和1mol H2O(g),发生上述反应,当反应达到平衡后,在其他条件不变时,再通入1mol H2O(g)和1mol CO(g)的混合气体,v正、v逆反应速率随时间t变化的示意图如下。 |
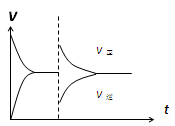
已知乙苯的结构简式为C6H5—C2H5,其一氯代物的同分异构体有5种。不用试写可知,它与3 mol H2发生反应后的一氯代物同分异构体数是()
| A.5 | B.6 | C.7 | D.8 |
25℃时有三瓶溶液:pH=3的盐酸、pH=3的醋酸溶液和pH=11的氢氧化钠溶液,下列说法正确的是()
| A.中和等体积pH=11的氢氧化钠溶液,所需pH=3醋酸溶液的体积大于pH=3盐酸的体积 |
| B.等体积pH=3盐酸和pH=3醋酸溶液中分别加入少量相同的锌粒,盐酸中锌粒先反应完 |
| C.当pH=3的醋酸溶液和pH=11的氢氧化钠溶液混合得到pH=7的溶液时,该 溶液中 c(Na+)大于c(CH3COO-) |
| D.25℃时pH=3的盐酸、pH=3的醋酸溶液中水电离出的c(H+)均为10-11mol/L |
某烃X,其比例模型中碳原子连接方式如图所示(氢原子均省略),下列说法正确的是()
| A.X的分子式C3H6 |
| B.完全燃烧时消耗氧气的体积是自身体积(相同条件)的4倍 |
| C.X与足量氯化氢发生加成反应时最多可得到两种产物 |
| D.无法确定X的分子式 |
恒温、恒压下,1 mol A和n mol B在一个容积可变的容器中发生如下反应:
A(g)+2B(g) 2C(g),一段时间后达到平衡,生成a molC。则下列说法中正确的是( )
2C(g),一段时间后达到平衡,生成a molC。则下列说法中正确的是( )
A.转化的物质A有a mol
B.起始时刻和达平衡时容器中的压强比为(1+n):(1+n - )
)
C.当υ正(A)=2υ逆(C)时,可判断反应达平衡
D.物质B的转化率为