现有A、B、C、D、E五种化合物,已知它们的阳离子有Al3+、Fe2+、K+、Ba2+、Ag+,阴离子有SO42-、Cl-、CO32-、NO3-、OH-现将它们分别配成0.1mol/L的溶液进行如下实验:
①测得C和E溶液显碱性,且碱性E>C
②A与C溶液混合后有白色沉淀和无色无味的气体生成,继续加入E溶液后溶液变澄清
③A溶液中加入D溶液后也出现白色沉淀,该沉淀不溶于稀硝酸
④B溶液中加入E溶液出现白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色
根据以上实验,回答下列问题:
(1) 写出五种物质的化学式
A , B , C , D , E 。
(2)按要求写出下列反应的反应方程式:
A与C 反应的离子方程式: 。
A中加入过量的E溶液后的离子方程式 。
B与E反应后的白色沉淀在空气中最终变成红褐色的化学方程式: 。
已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加D溶液,白色沉淀逐渐消失。
⑴.四种物质的化学式为:A、B、C、D。
⑵.现象③中所发生反应的离子方程式为:
、。
A~G各物质间的关系如下图,其中B、D为气态单质。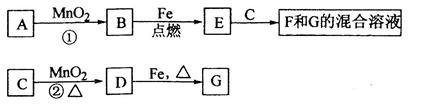
请回答下列问题:
(1)物质C和E的名称分别为、;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为;
若只能在加热情况下进行,则反应物A的化学式(分子式)为;
(3)反应②的化学方程式为 ;
;
(4)新配制的F溶液应加入以防止其转化为G。检验G溶液中阳离子的常用试剂是(填化学式),实验现象为。
关注饮用水,保证人民的生活质量。回答下列两个问题:
(1)饮用水中的NO3— 对人类健康会产生危害,为了降低饮用水中NO3—的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:
10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑+ 2H2O。请回答下列问题:
①上述反应中,元素的化合价升高,则该元素的原子(填“得到”或“失去”)电子。
②用“单线桥法”表示反应中电子转移的方向和数目:
10 Al+ 6 NaNO3 + 4 NaOH =" 10" NaAlO2 + 3 N2↑+ 2 H2O
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
。
②漂白粉的有效成分是(填化学式)。
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,离子方程式为。
请按要求书写下列反应方程式:
(1)用消石灰和氯化铵固体共热制取氨气,请写出其反应的化学方程式:
。
(2)常温下,二氧化硅与氢氟酸反应,请写出其反应的化学方程式:
。
(3)将红热的木炭投入到浓硫酸中,请写出其反应的化学方程式:
。
(4)氢氧化亚铁在空气中由白色经灰绿色变为红褐色,请写出其反应的化学方程式:
。
(5)氨的催化氧化,请写出其反应的化学方程式:
。
(6)将 氯气通入水中,请写出其反应的离子方程式:
氯气通入水中,请写出其反应的离子方程式:
。
(7)向氢氧化铝沉淀滴入氢氧化钠溶液至过量,请写出其反应的离子方程式:
。
(8)向FeCl2溶液中滴入氯水,请写出其反应的离子方程式:
。
(9)向硅酸钠溶液中通入过量的CO2,请写出其反应的离子方程式:
。
(10)将铜片放入在FeCl3溶液中,请写出其反应的离子方程式:
。
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。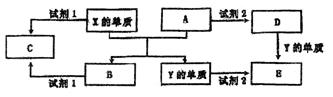
回答下列问题:
(1)X的单质与A反应的化学方程式是。
(2)若C溶液显碱性,则试剂1是液溶(写化学式):若C溶液显酸性,则显酸性的原因是(用离子方程式表示)。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是;
②写出D→E反应的离子方程式;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平): [来源:。