单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。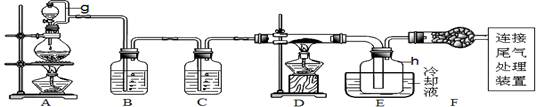
相关信息:①四氯化硅遇水极易水解;②SiCl4沸点为57.7℃,熔点为-70.0℃。请回答:
(1)写出装置A中发生反应的离子方程式 。
(2)装置C中的试剂是 ;装置F的作用是 ;
装置E中的h瓶需要冷却的理由是 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①反应的离子方程式: 。
②滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
③滴定前检验Fe3+是否被完全还原的实验操作是 。
下图是两个实验装置(铁架台等辅助仪器略去未画)②原混合物中碳酸钠的质量分数。
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
(1)如图 所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是,
所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是,
本实验所需玻璃仪器E规格为 mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度 的标准溶液 的标准溶液 |
B.长期贮存溶液 |
| C.用来加热溶解固体溶质 | D.量取一定体积的液体 |
(3)在配制NaOH溶液实验中其他操作均正确。若定容时仰视刻度线,则所配溶液浓度0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容则所配溶液浓度
0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为mL(计算结果保 留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
“化学多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生。下图所示就是一个“化学多米诺实验”,其中A~F装置中分别盛放的物质为:
| A.稀硫酸; | B.锌粒; |
| C.某溶液; | D.CaCO3固体;E、滴有紫色石蕊试液的蒸馏水;F、足量的澄清石灰水 |

请回答下列问题:
⑴反应开始后,若E中出现红色,F中有白色沉淀生成,则C中的物质可能是。
⑵装置D中的离子方程式,该反应的类型是,
装置F中的离子方程式。
⑶上图B~F装置中发生氧化还原反应的是(填编号)。
用单线桥表示出电子转移。
FeSO4?7H2O广泛用于医药和工业领域。
以下是FeSO4?7H2O的实验室制备流程图。
根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为(用离子方程式表示),反应Ⅰ需要加热数分钟,其原因是。
(2)废铁屑中含氧化铁,无需在制备前除去,理由是
(用离子方程式回答),。
(3)判断反应Ⅱ完成的现象是:。
以下是测定某补血剂(FeSO4?7H2O)中铁元素含量的流程图。根据题意完成下列填空: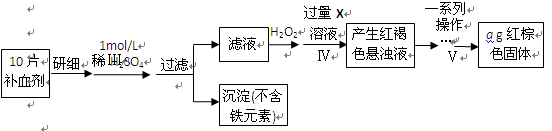
(4)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及。写出步骤Ⅳ的离子方程式:。
(5)步骤Ⅴ一系列操作依次是:①过滤②洗涤③④冷却⑤称量⑥恒重操作。操作⑥的目的是。
(6)假设实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示)。
I.仅用下列装置,检验木炭和浓硫酸反应产生的混和气体中含有SO2和CO2。在下列表格中填写对应的药品和实验现象。
| 实验装置 |
检验气体 |
试剂名称 |
实验现象 |
| A |
SO2 |
||
| B |
CO2 |
II.利用下列装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。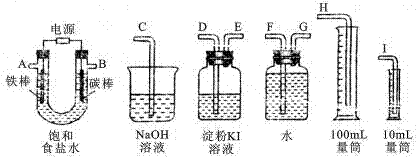
(1)将上面各仪器连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接______________,B接______________。
(2)请写出铁棒电极上发生的电极反应式__________________________。
(3)能说明氯气具有氧化性的实验现象是_______________________________。
(4)若U管中装入的饱和食盐水为50mL(电解前后溶液体积变化可忽略),当收集到的氢气为5.6mL(标准状况)时停止通电,摇匀U型管内的溶液,取20.00mL该溶液于锥形瓶内,用0.01mol/L的盐酸滴定时,滴定管起始读数为1.00mL,滴定终点时,滴定管的读数为_______ mL。