由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示: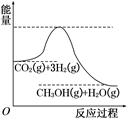
(1)上述反应平衡常数K的表达式为 ,温度降低,平衡常数K (填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)= 。
| t/min |
0 |
2 |
5 |
10 |
15 |
| n(CO2)/mol |
1 |
0.75 |
0.5 |
0.25 |
0.25 |
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是 (填写序号字母)
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
一种常用化学胶水的主要成分是聚乙烯醇,工业上以烃A为主要原料合成,其合成路线如下(某些反应条件略去):
已知:B的分子式为C2H4O,B的核磁共振氢谱中有两个峰,峰面积之比为3∶1;不饱和碳原子与羟基直接相连不稳定。请回答下列问题:
(1)A的结构简式为;
(2)聚乙烯醇中含有的官能团的结构简式为;
(3)反应Ⅱ的反应类型是;
(4)与CH3COOCH=CH2含有的官能团相同的同分异构体还有种;
(5)写出反应Ⅲ的化学方程式。
有位于周期表前四周期的A、B、C、D、E、F六种元素,其原子序数依次增大。已知A原子核外有三个未成对电子;A与B形成的一种化合物常温下是红棕色气体;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;F原子核外最外层电子数与C相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D四种原子的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)C的氯化物的熔点比D的氯化物的熔点(填“高”或“低”),理由是。
(3)E的最高价氧化物分子的空间构型是。
(4)基态F+离子的核外电子排布式是,F的高价离子与A的最常见氢化物形成的配离子的化学式为。
(5)Q分子是A2B的等电子体,Q的结构式为,Q分子的中心原子的杂化类型是。
(6)下图是B、F两元素组成的一种化合物的晶胞,其化学式为。
甲醇是一种重要的可再生能源,工业上可用CO和H2合成。
(1)已知:CO(g)+1/2O2(g)=CO2(g)△H=—283 kJ·mol—1
CH3OH(l)+3/2O2(g)=CO2(g) +2H2O(l)△H=—725kJ·mol—1
若要求得CO(g)+2H2(g)=CH3OH(l)的△H,还需要知道反应(用化学方程式表示)的焓变。
(2)在Cu2O/ZnO做催化剂的条件下,将CO(g)和H2(g)充入容积为2L的密闭容器中合成CH3OH(g),反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图。
根据题意回答下列问题:
①反应达到平衡时,平衡常数表达式K=;
升高温度,K值(填“增大”、“减小”
或“不变”)。
②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=。
③若其它条件不变,对处于Z点的体系,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法正确的是。
a.氢气的浓度与原平衡比减少 b.正、逆反应速率都加快
c.甲醇的物质的量增加 d.重新平衡时n(H2) /n(CH3OH)增大
④据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2有利于维持Cu2O的量不变,原因是:(写出相关的化学方程式并辅以必要的文字说明)。
CS2和S2Cl2都是硫的重要化合物,在工业上有广泛的用途。二者的部分性质如下:
| 熔点/℃ |
沸点/℃ |
密度/g·cm—3[来源 |
水 |
|
| CS2 |
—110.8 |
46.5 |
1.26 |
难溶 |
| S2Cl2 |
—76 |
138 |
1.75 |
水解 |
(1)①在 CS2+3Cl2=CCl4(g)+S2Cl2反应中,化合价没发生变化的元素是。
②在CS2和S2Cl2中,含有非极性键的是。
(2)以CS2或单质硫做原料与氯气反应都可以制得S2Cl2。下图是实验室里通过在熔融的单质硫中通入少量氯气的方法制取S2Cl2的装置(夹持装置、加热装置均已略去)。
①装置a中的试剂是,其作用是;
装置d的名称是,其作用是。
②该实验的操作顺序应是(用序号表示)。
A.加热装置c B.通入Cl2C.通冷凝水 D.停止通入Cl2
E.停止加热装置c
③f装置中的试剂是,其作用是。
A、B、C、D是中学化学中常见的单质, D为地壳中含量最多的金属;甲、乙、丙为化合物,其中甲为有磁性的黑色晶体,乙在常温常压下为无色液体。各物质的转化关系如下:
(1)组成D的元素在周期表中的位置是。
(2)若用一种反应类型概括上述转化中所涉及到的全部反应,该反应类型是。
(3)在上述电解反应中,阳极的电极反应式是。
(4)甲和D反应的化学方程式是。
(5)D的某种盐常用于净水,用离子方程式表示其净水原理。