X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是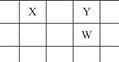
| A.5种元素中,原子半径最大的是W |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Y的简单阴离子比W的简单阴离子还原性强 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,某同学对该固体进行了如下实验
下列判断正确的是:
| A.气体甲一定是纯净物 |
| B.白色沉淀乙不一定是Al(OH)3 |
| C.固体X中一定存在 (NH4)2SO4、MgCl2 |
| D.固体X中一定存在FeCl2、AlCl3 |
Fe和Fe2O3的混合物共13.6g,加入150mL稀H2SO4,在标准状况下收集到1.12LH2,Fe和Fe2O3均无剩余。为中和过量的H2SO4,并使Fe元素全部转化为Fe(OH)2沉淀,消耗了200mL 3mol/L的NaOH溶液,则该H2SO4的物质的量浓度为
| A.2.25mol/L | B.2mol/L | C.4mol/L | D.0.6mol/L |
在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液褪色,其中发生反应的离子方程
式为:2MnO4- +16H+ + 5Na2O2 ="===" 2Mn2+ +5O2↑ + 8H2O + 10Na+ 下列判断正确的是:
| A.高锰酸钾是氧化剂,Na2O2既是氧化剂,又是还原剂 |
| B.反应的氧化产物只有氧气 |
| C.当反应产生标准状况下2.24 L O2时,反应转移的电子为0.1mol |
| D.通常所说的酸化的高锰酸钾溶液是指滴加了浓盐酸的高锰酸钾溶液 |
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
| 选项化合物 |
A |
B |
C |
D |
| Y |
CO2 |
Fe2O3 |
SiO2 |
FeCl3 |
| W |
MgO |
Al2O3 |
CO |
CuCl2 |
解释下列相应的实验事实方程式正确的是
| A.稀硫酸与氢氧化钡溶液恰好中和:Ba2++OH-+H+十SO42-= BaSO4↓+H2O |
B.测得0.1 mol/L氨水中C(OH-)为10-3 mol/L:NH3·H2O NH4++OH- NH4++OH- |
| C.在偏铝酸钠溶液中通入过量CO2出现白色沉淀:2AlO2-+ CO2 + 3H2O = 2Al(OH)3↓ + CO32- |
| D.碳酸氢钠溶液与过量石灰水混合出现白色沉淀:2HCO3-+ Ca2+ + 2OH- = CaCO3↓+ CO32-+2H2O |