某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是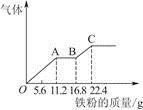
A.原混合酸中 物质的量浓度为2 mol/L 物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol/L |
下列说法正确的是
| A.制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 |
| B.向1 mL浓度均为0.05 mol·L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol·L-1的AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI) |
| C.0.1mol·L-1的NaOH溶液分别中和pH、体积均相等的醋酸和盐酸,所消耗NaOH溶液的体积:前者小于后者 |
| D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
电解法是处理工业废水的一种重要方法。如酸性含(Cr2O72-)废水就可以采用电解法进行无害化处理。电解时采用Fe作阳极,惰性电极作阴极。已知:①氧化性:Cr2O72->Fe3+;②Cr2O72-被还原生成Cr3+;③Ksp[Cr (OH)3]=6.3×10-31。下列说法正确的是
| A.阳极材料也可以是Cu |
| B.阴极每产生3molH2,则有1mol Cr2O72-被还原 |
| C.一段时间后溶液中发生反应Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O |
| D.电解最后阶段需要加碱,使溶液中的阳离子转化为沉淀 |
S-诱抗素能保持鲜花盛开,S-诱抗素的分子结构,如图,下列关于该物质说法正确的是
| A.S-诱抗素能发生酯化反应的官能团有2种 |
| B.S-诱抗素含有苯环、羟基、羰基、羧基、碳碳双键 |
| C.1 mol S-诱抗素与足量金属Na反应生成0.5 mol H2 |
| D.该化合物不能发生聚合反应 |
某有机物T的分子式为C5H12O4,0.1mol T与足量钠反应生成4.48L(标准状况)氢气。已知一个碳原子上连接两个-OH的有机物不稳定。则T的稳定结构(不考虑立体异构)有
| A.6种 | B.7种 | C.8种 | D.9种 |
设NA为阿伏加德罗常数的值,则下列说法正确的是
| A.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| B.向NH4Al(SO4)2稀溶液中逐滴加入过量Ba(OH)2溶液,离子方程式为:NH4++Al3++2SO42-+ 2Ba2++ 5OH-=2BaSO4↓+ AlO2-+ 2H2O+NH3•H2O |
| C.常温下,由水电离出的H+浓度为10-13mol·L-1的溶液中,Fe2+、Cl-、Na+、NO3-可能大量共存 |
| D.葡萄糖(C6H12O6)溶液中:SO42-、MnO4-、K+、H+ 可以大量共存 |