10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:___________________________
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确。试剂X是 。
A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 (填“甲”或“乙”)判断正确。
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH—浓度分别为amol /L和bmol /L,则a与b的比值= 。
市场销售的 某种食用精制加碘盐中含有碘酸钾
某种食用精制加碘盐中含有碘酸钾
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处) KIO3+KI+H2SO4=K2SO4+I2+H2O
KIO3+KI+H2SO4=K2SO4+I2+H2O
(2)上述反应生成的I2可用四氯化碳检验。碘的四氯化碳溶液呈色。
(3)向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,可以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是。
(4)已知: I2+2S2O32-=2I-+S4O62-.某学生为测定碘含量,称取一定质量的食盐,加适量蒸馏水使其完全溶解;
I2+2S2O32-=2I-+S4O62-.某学生为测定碘含量,称取一定质量的食盐,加适量蒸馏水使其完全溶解;
a.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
b.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断b中反应恰好完全依据的现象是。
②b中反应所产生的I2的物质的量是mol。
下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。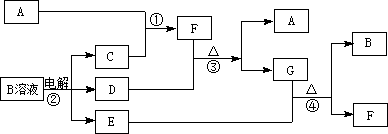
(1)写出化学式A,D,G,
写出电子式F;
(2)鉴定G中阳离子的实验方法和现象:_________________________________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式D+E③。
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目。
按下图装置实验,a、b、c、d均为惰性电极,A、B两烧杯中分别盛放NaOH溶液和足量CuSO4溶液。通电一段时间后,c电极质量增加6.4g,试回答: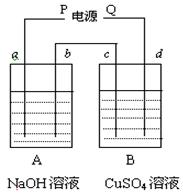
(1) 电源Q为________极;
(2) b极产生气体的体积为_______L(标准状况);电解一段时间后,A池中溶液的PH。(填“变大”“变小”或“不变”)
(3) d极上所发生的电极反应式:。
(4)B装置中电解反应的离子方程式为:。
已知2SO2 (g)+ O2(g) 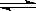 2SO3(g)△H =-196kJ·mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:高考
2SO3(g)△H =-196kJ·mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:高考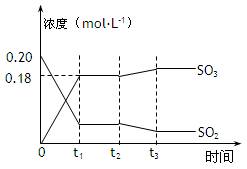
请回答下列问题:
(1)用O2表示2分钟内该反应的平均反应速率为mol·L-1·min-1。计算500℃时该反应的平衡常数K=。
(2)上图表示该反应在时刻t1达到平衡后,时刻t2因改变某个条件而发生变化的情况:
图中时刻t2发生改变的条件可能是(写一个即可)。
(3)在上述条件下起始装入的SO2和O2各2mol,达平衡后设SO2的转化率为x,列出求x的方程。(不必求出x)
(4)某温度时,该反应的平衡常数K=5000,则该温度500℃(填“>”、“<”、“=”)。
(5)500℃时,若起始装入的SO2、O2和SO3分别为0.2mol、y mol、wmol,达到平衡时各组分的含量与第(3)完全相同,则y=mol。刚开始时反应向(填“正”或“逆”)反应方向进行。
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
(1)若溶液中只溶解了一种溶质,该溶质的名称是,上述离子浓度大小顺序关系中正确的是(选填序号)。
(2)若上述关系中C是正确的,则溶液中溶质的化学式是。
(3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)
c(Cl-)。