V2O5是接触法制硫酸的重要催化剂,工业上生产V2O5的工艺流程如下:请回答下列问题: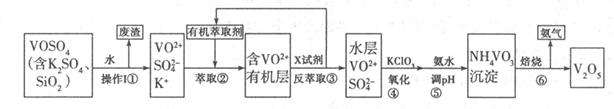
(1)步骤①所得废渣的成分是 (写化学式),它与NaOH溶液反应的离子反应方程式为 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+2nHA(有机层)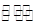 2RAn(有机层)+nH2SO4(水层),
2RAn(有机层)+nH2SO4(水层),
①实验室中步骤②、③使用的主要仪器是 。
②中萃取时必须加入适量碱,其原因是 。
(3)步骤③中X试剂为 ,步骤④的目的是 ,步骤⑤的离子方程式为 。
(4)该工艺流程中,可以循环利用的物质有 和 。
(1)填写下列实验操作主要仪器名称:
浓缩CuSO4溶液所用容器是___ ____;
分离酒精和水的受热容器是____________ _______;
石油的蒸馏装置中通冷却水的仪器是____ ____;
接受馏出产品的仪器是____ ______。
(2)填写下列实验过程的主要操作或方法的名称:
分离汽油和水的混合物 ;
提取碘水中的碘 ;
去除水中的沙子 ;
除去淀粉溶液里混有的氯化钾 ;
鉴别Fe(OH)3溶胶和碘酒溶液 。
(3)用自来水配制的AgNO3溶液,会出现浑浊。过滤出沉淀,向其中加入稀HNO3沉淀不溶解,请你分析该沉淀的成份是____________,说明自来水中含有_____________离子(用化学式符号填写),该反应的离子方程式为 。
下列五组物质,每组中有一种物质从某种角度分析与其它四种不同,请找出该物质填在后面的空白处:
(1)Fe、S、C、P ;
(2)HCl、H2SO4、HNO3、NaHSO4 ;
(3)空气、氢气、碘酒、盐酸 ;
(4)Ag2CO3、BaSO4、NaNO3、CaCO3 ;
(5)CuSO4、Fe(NO3)3、KMnO4、Na2CO3 ;
某工厂排出的废水中含有大量的Fe2+、Cu2+和SO42-.
Ⅰ、某校研究性学习小组设计如图流程以回收铜和硫酸亚铁.请回答: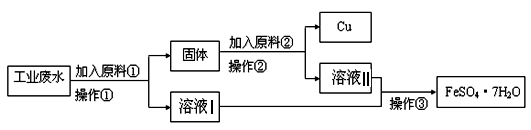
(1)反应①的离子方程式为 。
(2)操作①中用到的玻璃仪器是______ (填序号)。
a.烧杯 b.漏斗 c.玻璃棒 d.酒精灯
(3)固体成份是 (填名称)。
(4)原料②的名称为 。
Ⅱ、回收的铜可用于制备胆矾(CuSO4·5H2O)。,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2 2CuSO4 + 2H2O。制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。
2CuSO4 + 2H2O。制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。
①请分析2Cu+2H2SO4+O2 2CuSO4 + 2H2O反应中,氧化剂是 ,还原剂是 (填化学式)。
2CuSO4 + 2H2O反应中,氧化剂是 ,还原剂是 (填化学式)。
②用双线桥标出上述反应的电子得失。2Cu+2H2SO4+O2 2CuSO4 + 2H2O
2CuSO4 + 2H2O
Ⅰ、现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3 ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-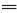 H2O,该反应的化学方程式为 。
H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水。医生常用胃舒平(主要成分氢氧化铝)来治疗,它与胃酸反应的离子方程式: 。
(4)上述十种物质中属于电解质的是: 。(填序号)
Ⅱ、阅读、分析下列两个材料: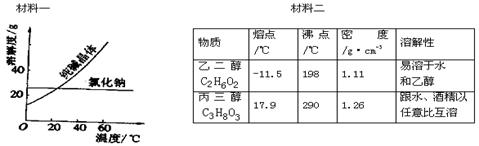
根据上述材料及课本知识,回答下列问题(每空只填一个字母选项):
| A.蒸馏法 | B.萃取法 | C.“溶解、结晶、过滤”的方法 | D.分液法 |
①分离汽油和水的最佳方法是 ;
②去除纯碱中的少量氯化钠杂质,最好应用 ;
③将乙二醇和丙三醇(乙二醇和丙三醇互溶)相互分离的最佳方法是 。
(1)相同物质的量的O2和CO分子个数比为________,所含氧原子的个数比为________,常温常压下下体积比:________。
(2)实验室要用Na2CO3配制500 mL 0.1 mol·L-1 Na2CO3溶液,回答下列问题:
①应该用托盘天平称取Na2CO3________g。
②需要的仪器:_____ ___,____ ____,___ ___,__ ,____ _____。
③若实验中有下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.转移液体时部分溅出 __________________;
B.定容时加水超过刻度线__________________;
C.最终定容时俯视观察液面 。