部分弱酸的电离平衡常数如下表:
| 弱酸 |
HCOOH |
HClO |
H2CO3 |
H2SO3 |
| 电离平衡常数 (25℃) |
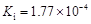 |
 |
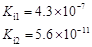 |
 |
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A.2ClO- + H2O + CO2 → 2HClO + CO32-
B.2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C.H2SO3 + 2HCOO- → 2HCOOH + SO32-
D.Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是…………………………………( )
A.H2O2既是氧化剂又是还原剂
B.H2O 既不是氧化产物又不是还原产物
C.H2SeO4既是氧化产物又是还原产物
D.氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸,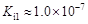 ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
HI+ H6TeO6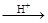 TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O
(6)若反应中生成的TeO2与Te的物质的量之比为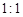 ,试配平上述化学方程式。
,试配平上述化学方程式。
现有以下物质:①NaCl晶体;②液态SO3;③纯硫酸;④汞;⑤BaSO4固体;⑥葡萄糖(C6H12O6);⑦酒精(C2H5OH);⑧熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是 。
(2)以上物质中属于电解质的是 。
(3)以上物质中属于非电解质的是 。
(4)以上物质中溶于水后形成的水溶液能导电的是 。
(1)写出下列物质在溶液中的电离方程式:
| HCl |
|
| H2SO4 |
|
| NaOH |
|
| Ca(OH)2 |
|
| KHSO4 |
|
| NaHCO3 |
(2)将下列物质①醋酸(CH3COOH)、②苛性钠、③氨水、④铁、⑤蔗糖、⑥水、
⑦CaCO3、⑧二氧化碳,根据表格内容进行填写。
| 属于电解质的是 (填序号,下同) |
|
| 属于非电解质的是 |
|
| 既不属于电解质也不属于 非电解质的是 |
三氯化铁晶体(FeCl3·6H2O)跟水反应生成的氢氧化铁胶体具有净水作用,三氯化铁被用作净水剂,并且具有实用价值。明矾[KAl(SO4)2·12H2O]也是具有实用价值的净水剂之一,城市自来水厂常用其在常温下对大量的水进行净化。
(1)如果选择适当的分类标准,可以将三氯化铁晶体和明矾这两种不同的物质归为同一类物质,请你来进行划分(只要答出其中两项即可):
①分类标准: ,物质类型名称 。
②分类标准: ,物质类型名称 。
(2)取某浑浊水50 mL盛在烧杯中,再向烧杯中加入适量的明矾粉末并用玻璃棒将水搅拌,发生的现象是
。
(3)食盐水和明矾溶液都是无色、澄清、透明的液体。对这两种液体进行鉴别方法很多,如果不用任何试剂进行鉴别,有关的方法、现象和结论是
。
已知实验室在加热条件下制取Cl2的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
(1)标准状况下生成Cl2的体积为 。
(2)反应的HCl的分子数为 。
(3)向反应后的溶液中加入足量的AgNO3溶液,可生成白色沉淀的质量为 。
(1)0.25 mol某固体A的质量是15 g,A的相对分子质量为 。
(2)在同温、同压、同体积的条件下,H2与气体A的质量之比是1∶8,A的摩尔质量为 。
(3)在25℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,A的摩尔质量为 。
(4)两个同容积的密封容器A、B,在25℃下,A中充入ag A气体,B中充入ag CH4气体,A与B内的压强之比是4∶11,A的摩尔质量为 。
(5)在同温、同压下,相同体积的CH4与气体A的密度之比为1∶4,A的摩尔质量为 。