化学学科需要借助化学专用语言描述,下列有关化学用语正确的是
A.CO2分子比例模型: |
B.NH4I的电子式: |
| C.乙醇的结构简式:C2H5OH |
| D.K+最外层电子排布式:4S24P6 |
化学与社会、生产、生活密切相关。下列说法正确的是
| A.65%的酒精用于消毒 | B.Al(OH)3可用于治疗胃酸过多 |
| C.明矾用于水的杀菌消毒 | D.从海水中提取可燃冰 |
25℃时,0.1 mol/L 的CH3COOH溶液 pH =3,0.1 mol/L的HCN溶液pH=4。下列说法正确的是
| A.CH3COOH与HCN均为弱酸,酸性:HCN > CH3COOH |
| B.25℃时,水电离出来的c(H+)均为 10-11mol/L的两种酸,酸的浓度:HCN > CH3COOH |
| C.25℃时,浓度均为0.1 mol/L 的CH3COONa和NaCN溶液中,pH大小:CH3COONa >NaCN |
| D.25℃时,pH均为3的CH3COOH与HCN溶液各100ml与等浓度的NaOH溶液反应,消耗NaOH溶液体积:CH3COOH >HCN |
利用下图所示装置进行实验,能实现实验目的的是(必要时可加热)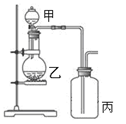
| 选项 |
实验目的 |
甲 |
乙 |
丙 |
| A |
制取并收集NH3 |
浓氨水 |
CaO |
H2O |
| B |
制取并验证C2H2可被KMnO4酸性溶液氧化 |
饱和食盐水 |
电石 |
KMnO4酸性溶液 |
| C |
制取并验证Cl2没有漂白性 |
浓盐酸 |
MnO2 |
干燥的红布条 |
| D |
制取并验证SO2具有漂白性 |
70%硫酸 |
Na2SO3 |
品红试液 |
某同学利用下图所示装置探究金属的腐蚀与防护条件。下列说法不合理的是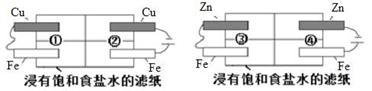
| A.①区Cu电极上产生气泡,Fe电极附近滴加K3[Fe(CN)6]后出现蓝色,Fe被腐蚀 |
| B.②区Cu电极附近滴加酚酞后变成红色,Fe电极附近滴加K3[Fe(CN)6]出现蓝色,Fe被腐蚀 |
| C.③区Zn电极反应式为Zn-2e-===Zn2+,Fe电极附近滴加K3[Fe(CN)6]未出现蓝色,Fe被保护 |
| D.④区Zn电极反应式为2H+ + 2e-===H2↑,Fe电极附近滴加K3[Fe(CN)6]出现蓝色, Fe被腐蚀 |