高炉炼铁过程中发生的反应: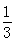 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
A.△H<0
B.该反应的平衡常数表达式是K=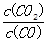
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
下列关于反应热的说法正确的是()
| A.当∆H﹤0时,表示该反应为吸热反应 |
B.已知C(s)+ O2(g)="CO(g)" △H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol O2(g)="CO(g)" △H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol |
| C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
常温下c(H+)最小的是()
| A.pH=0的溶液 | B.0.03 mol·L-1 H2SO4 |
| C.0.05 mol·L-1 HClO | D.0.05 mol·L-1的NaHSO4 |
对滴有酚酞试液的下列溶液,操作后颜色变深的是()
| A.明矾溶液加热 | B.CH3COONa溶液加热 |
| C.氨水中加入少量NH4Cl固体 | D.小苏打溶液中加入少量NaCl 固体 固体 |
某一反应在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为()
| A.大于25.3% | B.小于25.3% | C.等于25.3% | D.约等于25.3% |
下列说法正确的是()
| A.一定温度下,反应MgCl2(1)=Mg(1)+Cl2(g)的△H>0,△S>0 |
B.水解反应NH4++H2O NH3·H2O+H+达到平衡后,升 NH3·H2O+H+达到平衡后,升 高温度平衡逆向移动 高温度平衡逆向移动 |
C.铅蓄电池放电时的负极和充电时的阳极均发生还原 反应 反应 |
| D.对于反应2H2O2=2H2O+O2↑, 加入MnO2或升高温度都能加快O2的生成速率 |