镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下: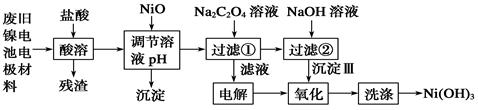
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。②K (Ni(OH)
(Ni(OH)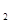 ): 5.0×10-16 ,K
): 5.0×10-16 ,K (NiC2O4): 4.0×10-10
(NiC2O4): 4.0×10-10
回答下列问题:
(1)酸溶后所留残渣的主要成份 (填物质名称)。
(2)用NiO调节溶液的pH,析出沉淀的成分为____________________(填化学式);用pH试纸测定某溶液pH的具体操作是 。
(3)写出加入Na2C2O4溶液后反应的化学方程式_____________________________。
(4)写出加入NaOH溶液所发生反应的离子方程式 ,该反应的平衡常数为 。
(5)沉淀Ⅲ可被电解所得产物之一 (填化学式)氧化生成Ni(OH)3 ,如何洗涤Ni(OH)3 沉淀?
。
(14分)已知有A、B、C、D、E五种短周期元素元素,其原子序数依次增大。F是常见的金属,在潮湿的空气中被腐蚀形成红棕色固体。A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正价与最低负价的代数和为6,D是同周期中离子半径最小的元素。
(1)五种元素中,金属性最强的元素在周期表的位置是________写出D元素的原子结构示意图________
(2)B元素的气态氢化物与其最高价氧化物对应的水化物化合,生成物的水溶液呈___性,原因________(离子方程式表示)上述化合物浓溶液滴加到Mg(OH)2悬浊液中,沉淀逐渐消失最后澄清,请解释澄清的原因______________________________________________
(3)含F的二价离子的酸性溶液,在空气中易被氧化变质,该过程的离子反应为:____________________
检验该二价离子没有被完全氧化的方法为:_______________________________
(4).E元素的最高价氧化物对应的水化物与D元素的最高价氧化物对应的水化物反应的化学方程式为____________________________________________________
(5分)化学实验是化学学科学习、探究的基础。
(1)下列描述错误的是_______.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解。
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液肯定存在的离子是:_______________
在②中产生的自色沉淀是:_________________
(13分)实验室以含有少量铁的粗铜粉和硫酸与硝酸的混合溶液为原料制备CuSO4·5H2O(胆矾)晶体。设计的工艺流程图如下: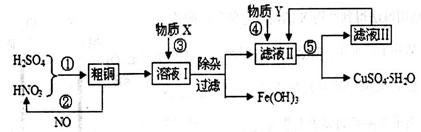
请回答下列问题:
(1)根据反应原理,操作①所需的混酸溶液中硝酸和硫酸的理论配比(物质的量之比)为________。操作②中需要把NO与_____气体混合通入水中,混入该气体的目的是__________________________(用化学方程式表示)。
(2)溶液I中存在一定浓度的Fe3+、Cu2+,在该浓度时生成氢氧化物沉淀的pH如下表。操作③中某学生设计物质X为H2O,若加水调整溶液pH,则Fe(OH)3开始沉淀的pH_______1.9(填“<”、“>”或“=”);而实际操作中一般不用此法调节溶液pH,其主要原因是___________________。
(3)操作④中物质Y为_______。查阅资料知CuSO4·5H2O的溶解度曲线如图所示,则操作⑤应采取的措施是蒸发浓缩、______________、过滤、洗涤、干燥等。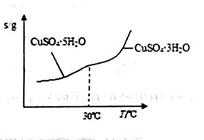
(4)为测定胆矾中结晶水的数目,称取25.0g胆矾品体在坩埚中加热,固体质量随温度升高而变化的曲线如图。
当固体质量为8.0g时,观察到固体完全呈黑色。请列式计算开始称取的胆矾中结晶水的数目。
(13分)SO2是主要大气污染物之一。工业上烟气脱硫的方法如下:
请回答下列问题:
(1)石灰—石膏法的流程如图: 。
。
该法原料便宜,产物有利用价值。写出氧化室中发生反应的化学方程式_______________。
(2)碱法的流程如图: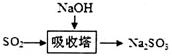 。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知:
。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知: )。
)。
(3)工业上在石灰—石膏法和碱法的基础上,结合两种方法的优点,设计出新的脱硫方案如下:

其中物质Y的化学式为_______,转化塔中反应的化学方程式是__________。
(4)最近利用碱法得到产物X的溶液电解制硫酸的工艺己被某些工厂采用。其装置如右图所示(电极为惰性电极)。阴极的电极反应式是__________,透过阴离子交换膜的离子主要为_________。该装置使X转化为硫酸的转化率不会超过________。
(13分)天然气的主要成分是甲烷,它是一种重要的燃料和基础化工原料。
(1)以甲烷和水为原料可制取甲醇。
①CH4(g)+H2O(g) CO(g)+3H2(g)△H=+206.0kJ/mol
CO(g)+3H2(g)△H=+206.0kJ/mol
②CO(g)+2H2(g) CH3OH(g)△H=—129.0kJ/mol
CH3OH(g)△H=—129.0kJ/mol
则CH4(g)+H2O(g) CH3OH(g)+H2(g)的△H=__________kJ/mol。
CH3OH(g)+H2(g)的△H=__________kJ/mol。
(2)用甲烷催化还原NOx为N2可消除氮氧化物的污染,写出反应的化学方程式_______。
(3)一定条件下,反应CH4(g)+H2O(g) CO(g)+3H2(g)可以制取合成氨的原料气H2。将1.0mol CH4和2.0 mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度的关系如图。已知100℃时达到平衡所需的时间是5min,则用H2表示的反应速率v(H2)=___________;该温度时的平衡常数K=__________,该反应的△H_______0(填“<”、“>”或“=”)。
CO(g)+3H2(g)可以制取合成氨的原料气H2。将1.0mol CH4和2.0 mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度的关系如图。已知100℃时达到平衡所需的时间是5min,则用H2表示的反应速率v(H2)=___________;该温度时的平衡常数K=__________,该反应的△H_______0(填“<”、“>”或“=”)。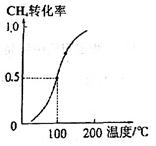
(4)某化学小组设计如图装置进行饱和NaCl溶液电解实验。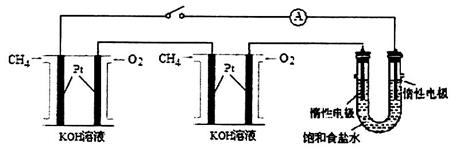
请回答下列问题:
已知每个甲烷燃料电池中盛有1.0L2.0 mol/L的KOH溶液。标准状况下,当每个燃料电池的负极通入甲烷的体积均为33.6L,且反应完全,则理论上电池溶液中c(K2CO3)_______c(KHCO3)(填“<”、“>”或“=”):最多能产生标准状况氯气的体积为________L。