某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示。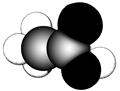
请根据其结构特点判断下列有关说法中正确的是
①该有机物的化学式为C2H4O2
②该有机物的水溶液呈酸性且酸性比碳酸强
③该有机物能发生酯化反应
| A.全部正确 | B.只有②错误 | C.只有③ | D.全部错误 |
如图所示,通电一段时间后,Cu电极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为100 mL,则通电前A池中原混合溶液Cu2+的浓度为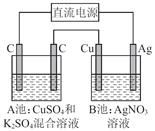
| A.0.05 mol/L | B.0.035 mol/L | C.0.025 mol/L | D.0.020 mol/L |
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )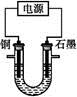
| A.铜电极连接电源正极 |
| B.黑色粉末X是铁粉 |
C.铜的相对原子质量的计算式是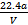 |
D.石墨电极上发生的反应是4OH--4e- O2↑+2H2O O2↑+2H2O |
图甲中电极均为石墨电极,下列叙述中正确的是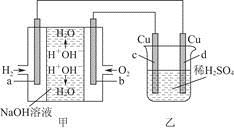
| A.电子沿a→d→c→d路径流动 |
| B.b极的电极反应为O2+4e-+4H+=2H2O |
C.通电初期乙中的总反应为Cu+H2SO4  CuSO4+H2↑ CuSO4+H2↑ |
| D.反应过程中,甲、乙装置中溶液的pH都逐渐减小 |
如图所示,Ⓐ为直流电源,Ⓑ为浸透饱和氯化钠溶液和酚酞试液的滤纸,Ⓒ为电镀槽。接通电路(未闭合K)后发现Ⓑ上的c点显红色。为实现铁片上镀铜,接通K后,使c、d两点短路。下列叙述不正确的是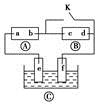
| A.b为直流电源的负极 |
| B.f极为阴极,发生还原反应 |
| C.e极材料为铁片,f极材料为铜片 |
| D.可选用CuSO4溶液或CuCl2溶液作电镀液 |
下列与装置有关的说法中正确的是
| A.图a中,随着电解的进行溶液中H+的浓度越来越大 |
B.图b中,Al电极作电池的负极,电极反应为Al-3e- Al3+ Al3+ |
C.图c中,发生的反应为Co+Cd2+ Cd+Co2+ Cd+Co2+ |
| D.图d中,K分别与M、N连接,Fe电极均受到保护不会腐蚀 |