NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,30 L pH=11的Na2CO3溶液中含有的OH-数为0.03NA |
| B.用含有0.1 mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C.25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D.100 mL 12 mol·L-l浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
一种碳纳米管(氢气)二次电池原理如右图,该电池的电解质为6mol·L—1KOH溶液,下列说法不正确的是()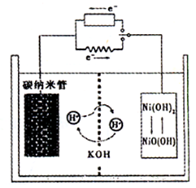
| A.储存H2的碳纳米管放电时为负极,充电时为阴极 |
| B.放电时负极附近pH减小 |
| C.放电时电池正极的电极反应为 NiO(OH)+H2O+e—===Ni(OH) 2+OH— |
| D.放电时,电池反应为2H2+O2===2H2O |
已知热化学方程式:2H2(g)+O2(g)===2H2O(g) ΔH1=-483.6 kJ/mol,则对于热化学方程式:2H2O(l)===2H2(g)+O2(g) ΔH2=b,下列说法正确的是( )
| A.热化学方程式中化学计量数表示分子个数 |
| B.该反应的ΔH2=+483.6 kJ/mol |
| C.|ΔH2|<|ΔH1| |
| D.|ΔH2|>|ΔH1| |
9.2g金属钠投入到足量的重水中,则产生的气体中含有()
| A.0.2mol中子 | B.0.4mol电子 |
| C.0.2mol质子 | D.0.4mol分子 |
下列化合物中,含有非极性键的离子化合物是
| A.Ba(OH)2 | B.H2SO4 | C.Na2O2 | D.CaCl2 |
下列说法正确的是 ( )
| A.10电子的离子对H2O的电离平衡均能产生影响 |
B. 与 与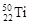 两种核素均是周期表第四周期主族元素 两种核素均是周期表第四周期主族元素 |
| C.IA族元素的原子半径比ⅦA族元素的原子半径大 |
| D.原子序数相差8的两种短周期元素,其周期序数相差1 |