下表中对离子方程式的评价不合理的是
| 选项 |
化学反应及离子方程式 |
评价 |
| A |
NaClO溶液中通入少量的SO2:ClO-+H2O+SO2===Cl-+SO42-+2H+ |
错误,碱性介质中不可能生成H+ |
| B |
用酸性高锰酸钾溶液滴定草酸:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O |
正确 |
| C |
NH4Al(SO4)2溶液中滴入几滴NaOH溶液:NH4++OH-===NH3·H2O |
错误,OH-首先和Al3+反应生成Al(OH)3沉淀 |
| D |
用惰性电极电解MgCl2溶液:2Mg2++2H2O 2Mg+O2↑+4H+ 2Mg+O2↑+4H+ |
正确 |
设nA为阿伏加德罗常数的数值。下列说法错误的是
| A.1mol NH3中含有3NA个N—H键 |
| B.0.1mol·L-1Na2CO3溶液中含有0.1NA个CO32- |
| C.标准状况下,11.2L CO2中含有NA个O原子 |
D.20g重水(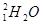 )中含有10NA个电子 )中含有10NA个电子 |
关于锂的结构和性质的判断,错误的是
①与水反应比钠剧烈②它的原子半径比钠小③它的氧化物暴露在空气中易吸收二氧化碳④它的阳离子的最外层电子数和钠的相同⑤它是还原剂
| A.①④ | B.②③ |
| C.③⑤ | D.① |
在100ml含等物质的量的HBr和H2SO3的溶液中通入0.025molCl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。则原溶液中HBr和H2SO3的浓度都等于
| A.0.16mol/L | B.0.02mol/L |
| C.0.20mol/L | D.0.25mol/L |
一定条件下,碘单质与砹单质以等物质的量进行反应,可得AtI。它与Zn、NH3都能发生反应,化学方程式分别如下:
2AtI+2Zn===ZnI2+ZnAt2 AtI+2NH3(l)===NH4I+NH2At。
则下列叙述正确的是
| A.ZnI2既是氧化产物,又是还原产物 |
B.ZnAt2既是氧化产物, 又是还原产物 又是还原产物 |
| C.AtI与液氨反应,AtI既是氧化剂,又是还原剂 |
| D.AtI与液氨反应,是自身氧化还原反应 |
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3 C 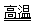 2 AlN + 3 CO ,则下列叙述正确的是
2 AlN + 3 CO ,则下列叙述正确的是
| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.上述反应中,每生成1molAlN需转移3mol电子 |
| C.AlN中氮元素的化合价为+3 |
| D.AlN的摩尔质量为41g |