合成肉桂酸异戊酯G(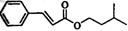 )的路线如下:
)的路线如下:

友情提示:
①B和C含有相同的官能团且C在标准状况下的气体密度为1.964g/L;
② 。
。
回答下列问题:
(1)A的结构简式为 ,D中含有的官能团的名称是 ;
(2)下列物质在一定条件下能与F反应的是 (填标号);
A.溴水 B.酸性KMnO4溶液 C.乙酸 D.新制氢氧化铜的悬浊液
(3)B和C反应生成D的化学方程式为 。
(4)E和F反应生成G的化学方程式为 ,反应类型为 。(各2分)
(5)A的同分异构体中含有苯环的共有 种(不考虑立体异构且包括A),其中与氯化铁不能发生显色反应且核磁共振氢谱有四组峰,峰面积之比为3:2:2:1的为______ (写结构简式)。(各2分)
铝土矿的主要成分是 ,含有杂质
,含有杂质 、
、 、
、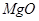 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:(1)图中涉及分离溶液与沉淀的实验方法是_________(填操作名称)。
(2)沉淀B的成分是____________(填化学式,下同),沉淀C的成分是____________;溶液D中所含的酸根离子是。
(3)沉淀F转化为物质M的化学方程式为________________________;
溶液D中通入过量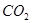 生成沉淀F的离子方程式为_______________________。
生成沉淀F的离子方程式为_______________________。
(4)能否将向溶液D中通入过量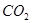 换成加入过量盐酸?(填 能 或 不能)
换成加入过量盐酸?(填 能 或 不能)
其理由是
甲、乙、丙三种物质之间有如下图所示的转化关系,其中甲物质为氧化物:
(1)若甲是不溶于水的白色固体,但既能溶于硫酸又能溶于氢氧化钠溶液,写出下列转化的方程式:
乙 丙的离子方程式_____________________________;
丙的离子方程式_____________________________;
丙 甲的化学方程式______________________________。
甲的化学方程式______________________________。
(2)若向乙溶液中加入KSCN溶液,混合溶液呈红色,则甲物质是________(填化学式)。甲 乙的离子方程式是______________________________。
乙的离子方程式是______________________________。
Ⅰ、实验室常用以下方法制取氯气:MnO2+ 4HCl(浓)  MnCl2+Cl2↑ + 2H2O,
MnCl2+Cl2↑ + 2H2O,
(1)用双线桥标出电子转移方向和数目。(在答题纸上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为,
被氧化HCl的质量为。
Ⅱ、科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为
对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化
合物。通过以上信息填空:
(1)维生素C具有(填氧化性或还原性)。
(2)上述过程中+5价砷类物质作为(填氧化剂或还原剂),+5价砷元素发生
反应(填氧化或还原);2mol +5价砷完全转化为 +3价砷,共转移个
电子(用NA表示阿伏加德罗常数)。
从石油裂解中得到的1,3—丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯。
(1)写出D的结构简式 。
(2)写出A的结构简式 。
(3)写出第⑦步反应的化学方程式 。
(4)写出富马酸的一种相邻同系物的结构简式 。
(5)写出第⑨步反应的化学方程式 。
(6)以上反应中属于消去反应的是 。(填入编号)
乳酸(CH3—CHOH—COOH)是人体生理活动的一种代谢产物,其聚合物(聚乳酸)是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。下图是工业上用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
物质H的结构简式为 ,回答下列问题:
,回答下列问题:
(1)写出下列物质的结构简式:C,F。
(2)上述反应①~⑦中,②是反应,⑥是反应。(填反应类型)
(3)写出下列反应的化学方程式:
①。
⑦。
(4)隐形眼镜的制作材料,应具有良好的光学性能、良好的透气性能和亲水性。一般采用G来制作隐形眼镜而不用H,其主要理由是。