现有4瓶没有标签的无色溶液,已知它们分别是稀盐酸、NaOH溶液、 溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。
溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。
| 实验步骤 |
实验现象 |
实验结论与解释 |
Ⅰ. 分别取四种待测液于4支试管中并编号,再分别向其中滴加无色的________溶液(如下图),振荡 |
①②③中的溶液均由无色变为红色 ④中无现象 |
①②③中溶液显________(填“酸”或“碱”)性 ④中的原试剂瓶中的溶液是________ |
| Ⅱ. 向上述所得①②③的溶液中分别加入已区分出的④溶液 |
三支试管中的溶液均由红色变为无色,①中还伴有的现象是________;②③中无其他现象 |
①中原试剂瓶中的溶液是Na2CO3溶液 步骤Ⅱ后①中的溶质可能是________________(除指示剂外) |
| Ⅲ. 向步骤Ⅱ后所得②③的溶液中,分别滴加过量的①中原试剂瓶中的溶液 |
②中先有无色气泡,出现白色沉淀,溶液由无色变为红色 |
②中原试剂瓶中的溶液是 溶液 溶液 |
| ③中的现象可能是_________ ___________________ |
③中原试剂瓶中的溶液是NaOH溶液 |
(10四川达州16)已知碳酸易分解,草酸与碳酸有相似的化学性质,在受热的条件下草酸也会分解,仅生成三种氧化物。我校研究性学习小组对此展开探究:
[提出问题] 生成的三种氧化物是什么?
[查阅资料] 无水硫酸铜是一种白色粉末物质,遇水变成淡蓝色硫酸铜晶体。化学方程式为:
CuSO4(白色粉末)+5H2O= CuSO4·5H2O(蓝色晶体)
[提出猜想] 生成的氧化物中有H2O、CO2和CO。
[实验探究] 张亮将生成的气体,依次通过如图所示装置,验证猜想。
⑴观察到A中_________,证明生成物中有水。
⑵B中澄清石灰水变浑浊,证明______________________。
⑶D中红色粉末是______(填化学实验现象)__________________。
[交流讨论]
陈军认为:张亮不需要E装置也能够推断出生成物中有一氧化碳。你是否支持陈军的观点:(填“支持”或“不支持”),请说出你的理由:________________________________
陈军还认为:从环保的角度来看,此装置有一个缺陷,请你指出该缺陷:_______,处理的方法是_______________________。
(10四川达州15)纯碱(Na2CO3)是一种重要的盐类物质,在化学工业中用途极广。工业上通常用氨碱法来生产。小红同学为探究纯碱的化学性质进行了猜想,并设计实验进行验证。请你帮助她将下列实验报告填写完整。
| 猜想 |
实验操作 |
实验现象 |
结论(或化学方程式) |
| 猜想一:Na2CO3溶液显碱性 |
取少量Na2CO3溶液于试管中,滴入2-3滴酚酞试液,振荡 |
溶液显碱性 |
|
| 猜想二:能与酸反应 |
取少量溶液于试管中,然后滴加稀盐酸 |
有大量气泡产生 |
化学方程式 |
| 猜想三:能与Ca(OH)2反应 |
向盛有少量Na2CO3溶液于试管中,滴加澄清石灰水 |
产生白色沉淀 |
化学方程式 |
| 猜想四:能与BaCl2反应 |
产生白色沉淀 |
Na2CO3+BaCl2=BaCO3↓+2NaCl 反应的基本类型为 |
[交流与反思] 若用稀硫酸代替稀盐酸进行实验,是否与猜想二相同?____(填“是”或“否”)。
(10广东省23)同学们在学碱的化学性质时,做了一个如下图所示的甲乙两个实验。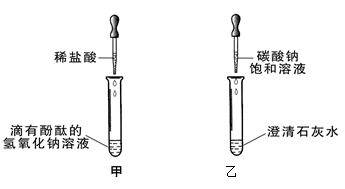
(1)写出乙实验的化学反应方程式______________________________,反应过程中产生的现象是________________________________。
实验结束后,甲、乙两个同学将废液倒入实验室的废液缸,结果发现废液浑浊并呈红色,产生疑问。
【提出问题】 废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和_______(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是_______________。(写一种猜想)
【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。
【反思拓展】 在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑________。
(10广东省19)2010年春节联欢晚会上,刘谦的魔术表演激起了人们强烈的好奇心,并在全国范围内掀起了魔术表演的热潮。在学校科技节活动中,一位九年级同学给低年级同学表演了一组化学小魔术,请你利用所学化学知识揭开其中之谜。
魔术一“奇花变色”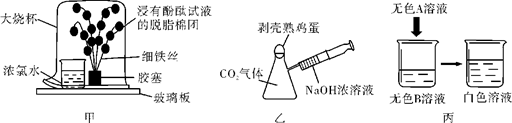
道具如图甲所示,该魔术可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为色。该魔术中没有涉及的性质是(填字母序号)。
A.氨分子是不断运动的 B.氨分子有一定质量
C.浓氨水具有挥发性 D.氨气的水溶液显碱性
魔术二“瓶吞鸡蛋”
道具如图乙所示,将注射器中NaOH浓溶液注入瓶中,片刻后会看到鸡蛋被“吞”入瓶中。该魔术中涉及的化学反应为________________(用化学方程式表示)。
魔术三 “‘清水’变‘牛奶’”
道具如图丙所示,当A溶液加到烧杯中,无色溶液变成白色浊液。若A为酸溶液,则A、B的可能组合:A为;B为(答案合理即可)。(只需写一组)
.鼠妇(如图甲)喜欢生活在阴暗的地方。在探究“光对鼠妇生活的影响”时,有同学发现用不同的瓶装收集到的鼠妇时,瓶内的明暗程度可能会影响实验的结果。因此,又做了如下实验:八个研究小组在野外阴暗的地方各自收集了10只鼠妇,第一组至第四组将鼠妇装在无色透明的塑料瓶中,第五组至第八组将鼠妇装在褐色的瓶中,带回实验室。实验时,各小组都把10只鼠妇随机均分为两份,放在如图乙所示的纸盒中,阴暗处中央放5只,明亮处中央放5只,然后观察鼠妇的分布。下表是各小组在几分钟后观察到的鼠妇分布数及平均值: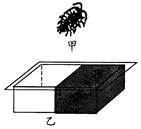
| 无色瓶 |
褐色瓶 |
|||||||||
| 一组 |
二组 |
三组 |
四组 |
平均值 |
五组 |
六组 |
七组 |
八组 |
平均值 |
|
| 明亮处/只 |
8 |
7 |
9 |
8 |
8.0 |
1 |
2 |
1 |
3 |
1.8 |
| 阴暗处/只 |
2 |
3 |
1 |
2 |
2.0 |
9 |
8 |
9 |
7 |
8.2 |
(1)观察上表中第一组到第四组的实验数据,可以得出“鼠妇喜欢明亮处”的结论,分析其主要原因是在回实验室的路上,用无色瓶带回的鼠妇已经与明亮环境相;
(2)为了减少对“光对鼠妇生活影响的实验”的干扰,在将收集到的鼠妇带回实验室时应选用瓶。