分冬青油是天然香料之一,其主要成分为水杨酸甲酯,可由水杨酸(邻羟基苯甲酸)和甲醇作原料在浓硫酸催化下酯化而得。
实验步骤:
Ⅰ.如图,在100 mL三口烧瓶中放入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯,再小心地加入8 mL浓硫酸,摇动混匀:加入1~2粒沸石,装上回流冷凝管在石棉网上保持85—95℃,加热回流1.5-2小时: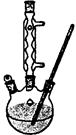
Ⅱ.待装置冷却后,分离出甲醇,向烧瓶中加入50 mL,水,然后转移至分液漏斗,分出下层产物,弃去上层水层,有机层再倒入分液漏斗中;依次用50 mL5%NaHCO3溶液洗1次(溶液呈弱碱性),30 mL水洗一次(产物皆在下层),有机层得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分。产品经0.5 g无水CaCl2干燥后称重。
常用物理常数: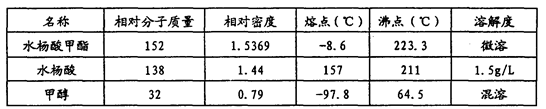
请根据以上信息回答下列问题:
(1)制备冬青油的化学方程式为______________。
(2)制备冬青油时,最合适的加热方法是_______________。实验中加入甲苯作带水剂的目的是____________________。
(3)反应结束冷却后,分离甲醇的操作是:___________________;
(4)在提纯粗产品的过程中,用碳酸氢钠溶液洗涤主要除去的杂质是____________:若
改用氢氧化钠溶液是否可以____________(填“可以”或“不可以”),其原因是________________。
(5)检验产品中是否含有水杨酸的化学方法是__________________。最终称得产品的质量为4.2 g,则所得水杨酸甲酯的产率为___________(保留两位有效数字)。
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下: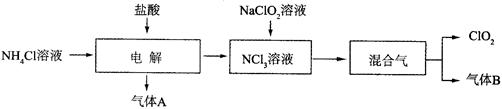
已知:①NCl3是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似氯气的刺激性气味,自然爆炸点为95℃,在热水中易分解,在空气中易挥发,不稳定。
②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为。
实验室制备气体B的化学方程式为,为保证实验的安全,在电解时需注意的问题是:①控制好生成NCl3的浓度;②。
(2)NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;
步骤2:量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30 min。
步骤3:以淀粉溶液作指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。
(已知I2+2S2O32-=2I-+S4O62-)
①上述步骤3中滴定终点的现象是;
②根据上述步骤可计算出原ClO2溶液的浓度为g /L(用含字母的代数式表示)。
氨气常用作致冷剂及制取铵盐和氮肥,是一种用途广泛的化工原料。(1)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
①曲线a对应的温度是。
②关于工业合成氨的反应,下列叙述正确的是(填字母)。
A.及时分离出NH3可以提高H2的平衡转化率
B.加催化剂能加快反应速率且提高H2的平衡转化率
C.上图中M、N、Q点平衡常数K的大小关系是K(M)= K(Q) >K(N)
③M点对应的H2转化率是。
(2)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。
①当氨水中所含氨的物质的量3mol,吸收标准状况下44.8 L SO2时,溶液中的溶质为。
②NH4HSO3溶液显酸性。用氨水吸收SO2,当吸收液显中性时,溶液中离子浓度关系正确的是(填字母)。
a.c(NH4+) = 2c(SO32-) + c(HSO3-)
b.c(NH4+)> c(SO32-)> c(H+)= c(OH-)
c.c(NH4+)+ c(H+)= c(SO32-)+c(HSO3-)+c(OH-)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,下图是供氨水式燃料电池工作原理:
①氨气燃料电池的电解质溶液最好选择(填“酸性”、“碱性”或“中性”)溶液。
②空气在进入电池装置前需要通过过滤器除去的气体是。
③氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池正极的电极反应方程式是。
[化学——选修2]化学与技术:(15分)硫酸是重要的工业原料.工业上生产硫酸主要分为造气、催化氧化、吸收三个阶段,其生产流程图如下: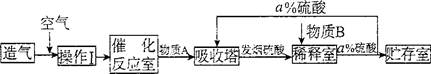
(1)操作I的内容是,此操作目的是.物质B是.a=。
(2)工业上既可用硫黄也可用硫铁矿(FeS2)造气,若使用硫铁矿造气.另一产物是一种常见的红棕色固体.写出用硫铁矿造气时反应的化学方程式。
(3)催化反应室中的反应是一个气体体积缩小的反应.增大压强有利于反应向右进行.但实际生产却是在常压下进行的.原因是。
(4)工业生产中常用氨一硫酸法进行尾气脱硫,以达到消除污染、废物利用的目的.用两个化学方程式表示其反应原理。
(5)若用等质量的硫黄、FeS2生产硫酸.假设原料的总利用率均为90%.则二者得到硫酸的质量比为。
(13分)硫、碳、氮等元素及其化合物与人类的生产生活密切相关,其中.硫酸、氨气、硝酸都是重要的化工原料.而SO2、NO、NO2、CO等相应氧化物又是主要的环境污染物:
(1)过度排放CO2会造成“温室效应”,而煤的气化是高效、清洁利用煤炭的重要途径。煤综合利用的一种途径如图所示。
已知:C(s)+H2O(g)=CO(g)+H2(g) AH1= +131.3 kJ·mol-
C(s)十2H2O(g)=CO2(g)+2H2(g) AH2=" +90" kJ·mol-
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是。
(2)298 K时.将氨气放入体积固定的密闭容器中使其发生分解反应。当反应达到平衡状态后.改变其中一个条件X,Y随X的变化符合图中曲线的是(填字号):
a.当X表示温度时,Y表示氨气的物质的量
b.当X表示压强时.Y表示氨气的转化率
c.当X表示反应时间时.Y表示混合气体的密度
d.当x表示氨气的物质的量时.Y表示某一生成物的物质的量
(3)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染.必须经脱除达标后才能排放:能作脱除剂的物质很多.下列说法正确的是(填序号):
a.用H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
d.用尿素[CO(NH2)2]作脱除剂.在一定条件下能有效将NOx氧化为N2
(4)在压强为O.1 MPa条件下,容积为V L的密闭容器中,amol CO与2amol H2在催化剂作用下反应生成甲醇。反应的化学方程式为CO(g)+2H2(g)  CH3OH(g),CO的平衡转比率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转比率与温度、压强的关系如图所示,则:
①P1P2(填“>”“<”或“=”)。
②在其他条件不变的情况下,向容器中增加a molCO与2amol H2.达到新平衡时.CO的转化率(填“增大””减小”或“不变”.下同),平衡常数.
③在P1下、100℃时,CH3OH(g)  CO(g)十2H2(g)的平衡常数为(用含a、V的代数式表示)。
CO(g)十2H2(g)的平衡常数为(用含a、V的代数式表示)。
(5)①常温下.若将2 mol NH3(g)和l mol CO2(g)通入1 L水中.可得pH=10的溶液,则该溶液中浓度最大的阴离子是;
②常温下,将0.01 mol·L- NaOH溶液和0.01 mol·L-(NH4)2SO4溶液等体积混合.所得溶液pH为10,那么该混合液中c(Na+)+c(NH4+)=mol·L一(填准确代数式.不能估算)。
铜、铝、硫及其它们的化合物应用广泛,如Cu可用作催化剂、制作印刷电路铜板等。
Ⅰ.铜的冶炼:工业上以辉铜矿为原料,采用火法熔炼工艺生产铜。
火法炼铜的方程式为:,该工艺的中间过程会发生反应2Cu20+辉铜矿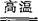 6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为。
6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为。
Ⅱ.粗铜精炼:利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是。
| A.电解时以精铜作阳极 |
| B.电解时阴极发生氧化反应 |
| C.粗铜连接电源负极,其电极反应是Cu一2e—=Cu2+ |
| D.电解后.电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
E.整个过程溶液中的Cu2+浓度减少
Ⅲ.铜及其化合物的性质探究:
将洁净的铜丝放在火焰上加热.并趁热插入到乙醇中,铜丝表面的现象为,
发生的反应为。
Ⅳ.无水氯化铝是一种重要的化工原料。利用明矾石:K2SO4·A12(SO4)3·2A1203·6H20]制备无水氯化铝的流程如下: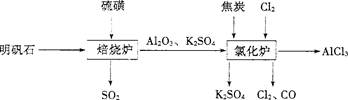
(1)验证焙烧炉产生的气体含有SO2的方法是。
(2)吸收焙烧炉中产生的S02,下列装置合理的是(填代号)。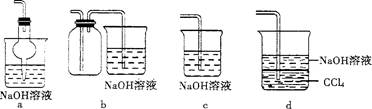
(3)氯化炉中发生反应的化学反应方程式为。
(4)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要捕述实验步骤、现象和结论)。
仪器自选;可供选择试剂如下:①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某实验小组设计了电化学方法进行二氧化硫的回收利用。利用电化学法将尾气中的SO2气体转化为 氮肥硫酸铵,模拟装置如图: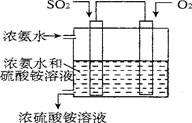
试写出SO2气体发生的电极反应式为。