空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。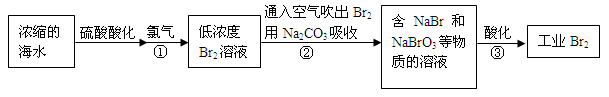
(1)NaBr的电子式是 。
(2)反应①是将Br—转化为Br2,反应①的离子方程式是 。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是 。
(4)反应②的化学方程式是 。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是 mol。
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中 (填字母)。
a.通入HBrb.加入NaBr溶液 c.加入Na2CO3溶液 d.加入Na2SO3溶液
在一密闭容器中发生反应N2+3H2 2NH3。达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
2NH3。达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
回答下列问题:
(1)t1、t2、t3时刻分别改变的一个条件,t1时刻 t3时刻 t4时刻 。
(2)氨的百分含量最高的时间段是 。
(3)如果在t6对刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化情况;
(4)实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1。

在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图。
有可逆反应Fe(s)+CO2(g)  FeO(s) + CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K="2.2" 。
FeO(s) + CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K="2.2" 。
(1)能判断该反应达到平衡状态的依据是 (双选,填序号)。
A.容器内压强不变了 B.c(CO)不变了 C.v正(CO2)=v逆(CO) D.c(CO2)=c(CO)
(2)该反应的正反应是_____________(选填“吸热”、“放热”)反应。
(3)写出该反应的平衡常数表达式______________。若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0 mol/L,则该温度下上述反应的平衡常数K=______________(保留二位有效数字)。
(4)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,反应混合气体中CO2的物质的量分数如何变化(选填“增大”、“减小”、“不变”)。
①升高温度________________;②再通入CO_________________。
(5)该反应的逆反应速率随时间变化的关系如图:
①从图中看到,反应在t2时达平衡, 在t1时改变了某种条件,改变的条件可能是(填序号)
__ ___。(单选)
A.升温 B.增大CO2浓度
②如果在t3时从混合物中分离出部分CO,t4~ t5时间段反应处于新平衡状态,请在图上画出t3~ t5的V(逆)变化曲线
氨可用于制取氨水、液氮、氮肥(尿素、碳铵等)、硝酸、铵盐、纯碱等,因此被广泛应用于化工、轻工、化肥、制药、合成纤维、塑料等行业中,最重要的化工产品之一。
(1)以甲烷为原料可制得合成氨气用的氢气。图1是一定温度、压强下,CH4(g)与H2O(g)反应生成CO(g)和2 mol H2(g)的能量变化示意图,写出该反应的热化学方程式 (△H用E1、E2、E3表示)。
(2)CO可使合成氨的催化剂中毒而失去活性,因此工业上常用乙酸二氨合铜(I)溶液来吸收原料气体中的CO,反应原理: [Cu(NH3)2CH3COO](l)+ CO(g)+NH3(g) Cu(NH3)3] CH3COO·CO(l) △H<0,吸收后的乙酸铜氨溶液经过适当处理后可再生而恢复其吸收CO的能力,则再生的适宜条件是 (填字母序号)。
Cu(NH3)3] CH3COO·CO(l) △H<0,吸收后的乙酸铜氨溶液经过适当处理后可再生而恢复其吸收CO的能力,则再生的适宜条件是 (填字母序号)。
| A.高温、高压 | B.高温、低压 | C.低温、低压 | D.低温、高压 |

(3)已知N2(g)+ 3H2  2NH3(g)△H=-94.4kJ·mol-1,恒容时,体系中各物质浓度随时间变化的曲线如图2所示,各时间段最终均达平衡状态。
2NH3(g)△H=-94.4kJ·mol-1,恒容时,体系中各物质浓度随时间变化的曲线如图2所示,各时间段最终均达平衡状态。
①在2L容器中发生反应,前20min内,ν(NH3)= ,放出的热量为 。
②25 min时采取的某种措施是 。
③时段III条件下反应的平衡常数为 。(保留3位有数字)
(4)用氨气制取尿素[CO(NH2)]的反应为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) △H<0。某温度下,向容器为100mL的密闭容器中通入4 mol NH3和2molCO2,该反应进行到40s时,达到平衡,此时CO2的转化率为50%。图3中的曲线表示在前25s内NH3的浓度随时间的变化。若反应延续至70s,保持其他条件不变的情况下,请在图3中用实线画出使用催化剂后c(NH3)随时间的变化曲线。
CO(NH2)2(l)+H2O(g) △H<0。某温度下,向容器为100mL的密闭容器中通入4 mol NH3和2molCO2,该反应进行到40s时,达到平衡,此时CO2的转化率为50%。图3中的曲线表示在前25s内NH3的浓度随时间的变化。若反应延续至70s,保持其他条件不变的情况下,请在图3中用实线画出使用催化剂后c(NH3)随时间的变化曲线。
选择适宜的材料和试剂设计一个原电池,以便完成下列反应: 2FeCl3+Cu 2FeCl2+CuCl2。画出原电池的示意图并写出电极反应。
2FeCl2+CuCl2。画出原电池的示意图并写出电极反应。
下图是自然界中部分自然现象和人类活动的图片,请分析它们为什么会污染大气?
___________________________________