红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。
提出问题:久置固体的成分是什么?
查阅资料:铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
作出猜想:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。
久置固体中可能含有Ca(OH)2的原因是:
用化学方程式表示 。
实验探究1:甲同学的方案(见下表)。
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 |
固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 |
固体中一定含有 和氢氧化钙 |
| (2)另取少量固体放于试管中,滴加足量 的 |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 |
固体中一定含有 , 一定不含有Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清石灰水中 |
|
固体中一定含有CaCO3 |
实验质疑:(1)乙同学认为甲同学的实验中的实验中不能得出一定含有Ca(OH)2的结论,理由是 。
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是 。
实验探究2:乙、丙同学设计如下图所示实验方案继续验证。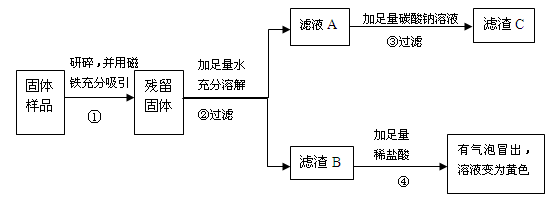
(1)③中反应的化学方程式是 。
(2)乙、丙同学实验中又能得出固体样品中一定还含有 ,
仍有一种物质不能确定,该物质是 。
【2015年江苏省盐城市】实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
【发现问题】该样品中含有哪些物质?
【查阅资料】①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性碱
③CO2在饱和的NaHCO3溶液中几乎不溶解
【提出猜想】猜想Ⅰ:NaOH猜想Ⅱ:Na2CO3 猜想Ⅲ:NaOH和Na2CO3
【设计实验】
| 实验操作 |
实验现象 |
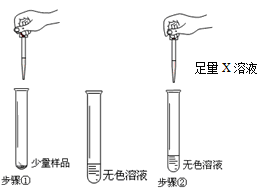 |
步骤①:样品全部溶解 步骤②:观察到现象A |
【收集证据】(1)若现象A是有气泡产生,则X溶液为 ,则 (填“猜想Ⅰ”、“猜想Ⅱ”或“猜想Ⅲ”)不成立.
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生沉淀的化学方程式是 ,取反应后的上层清液,测定其PH,当PH 7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
【定量分析】确定部分变质样品中Na2CO3的质量分数.
兴趣小组的同学用如图所示装置进行实验.
步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL.(已知:室温条件下,CO2的密度为1.6g•L﹣1)
(1)B装置集气瓶内原有的空气对实验结果 (填“有”或“没有”)影响.饱和NaHCO3溶液如果用水代替,则所测CO2体积 (填“偏大”、“偏小”或“不变”).
(2)计算该样品中Na2CO3的质量分数(写出计算过程,计算结果保留一位小数)
【实验反思】有同学指出,上述三种猜想并不全面,请再提出一种猜想 .
【2015年广西省玉林、防城港市】玲玲在学习复分解反应时,对复分解反应的条件产生了兴趣,于是她和小组内的同学仅用以下药品展开了探究活动。
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、氯化钠溶液、酚酞溶液
【提出问题】他们要探究的问题是 。
【查阅资料】硝酸钡溶液显中性,且Ba2+有毒。
【实验探究】玲玲用上述物质做了下列几组实验
【记录和解释】
(1)组合①、②、⑤均无明显现象,其中组合 与另外两组的实质不同。为证明该不同之处,玲玲在实验过程中使用了酚酞溶液。
(2)请写出组合③的化学方程式 。
【实验结论】他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有沉淀
或 生成时,复分解反应才可以发生。
【拓展延伸】实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。为了确定沉淀和清液的成分,继续展开探究。
【实验1】探究沉淀的成分。
【提出猜想】I.沉淀只有硫酸钡II.沉淀只有碳酸钡III沉淀中含有硫酸钡和碳酸钡
梅梅取少量沉淀于试管中,滴加 (请补充完整实验操作和观察到的现象),证明了猜想III是正确的。
【实验2】探究清液的成分。
①取少量清液于试管中,向其中滴加几滴硝酸钡溶液,无明显现象。
②另取少量清液于另一只试管中,滴加几滴 ,有白色沉淀产生。
【解释与结论】探究活动结束后,小组内成员通过讨论分析,一致认为清液中含有的离子是
(指示剂除外)。
【处理废液】为了防止污染环境,玲玲向废液缸中加入适量的 ,对废液进行处理后,将固体回收进一步处理,溶液排放。
【交流与反思】根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐 (写化学式)。
【2015年贵州省黔东南州】某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答先关问题:
【查阅资料】
信息①:相同条件下,碳酸钠溶液比碳酸氢钠溶液碱性强
信息②:NaHCO3在2700C时,完全分解转化成Na2CO3,而NaHCO3不易分解
【实验过程】
(1)按有图所示进行实验,只观察到烧杯B中的石灰石变浑浊,小试管内壁出现水珠,写出小苏打分解的化学方程式 。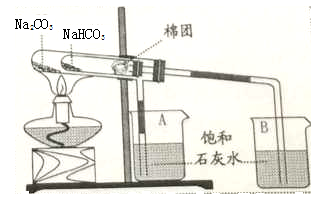
(2)充分利用信息知识,区分无色Na2CO3溶液
与NaHCO3溶液最简单的方用是 。
A、加热 B、pH试纸 C、稀盐酸
【实验过程】
(3)可用小苏打治疗轻度胃酸(主演含盐酸)过多的病人,其原因是:
【2015年江苏省泰州市】某校九(1)班同学举行“是真的吗?”化学主题活动,请你和蓓蓓一起探究。
话题1:能被磁铁吸引的物质一定是铁单质吗?
【实验验证】①将细铁丝在纯氧中完全燃烧,主要反应的化学方程式为 。
②将反应后的黑色固体用磁铁检验,能被吸引。
【实验结论】能被磁铁吸引的物质 (填“一定”或“不一定”)是铁单质。
话题2:含有Ba2+的盐一定有毒吗?
【社会调查】在医院检查胃肠疾病时,病人需服用“钡餐”(主要成分为BaSO4)。
【调查结论】“含有Ba2+的盐一定有毒”这句话是 (填“真的”或“假的”)。
【交流反思】若误服碳酸钡(BaCO3),胃酸的主要成分 (填化学式)会与之发生反应,形成可溶性钡盐,使人体内蛋白质变性而中毒,此时可服用 (填一种即可)解毒。
话题3:向某溶液中先滴加足量稀硝酸,再滴加氯化钡溶液,若产生白色沉淀,原溶液中一定含有SO42-吗?
【实验回顾】向硝酸银溶液中先滴加稀硝酸,再滴加氯化钡溶液,也产生白色沉淀,反应的化学方程式是 。
【实验结论】向某溶液中先滴加足量稀硝酸,再滴加氯化钡溶液,若产生白色沉淀,原溶液中不一定含有SO42-。
【拓展实验】向硫酸钠溶液中先滴加足量稀硝酸,再滴加氯化钡溶液,也产生白色沉淀。
【查阅资料】①硝酸具有强氧化性。向Na2SO3溶液中滴加稀硝酸时,发生如下反应:
2HNO3(稀)+3Na2SO3=3Na2SO4+2NO↑+H2O
②含有SO32-的盐统称为亚硫酸盐,亚硫酸盐都能与盐酸反应生成二氧化硫气体。
【交流反思】①向某一种钠盐溶液中先滴加足量稀硝酸,再滴加氯化钡溶液,产生白色沉淀。原溶液中阴离子可能是SO42-,还可能是 (填离子符号)。
②下列实验方案中,能证明溶液里含有SO42-的是 (填“A”或“B”)。
A.取样,先滴加氯化钡溶液,产生白色沉淀,再滴加稀盐酸,沉淀不溶解
B.取样,先滴加稀盐酸,无明显现象,再滴加氯化钡溶液,产生白色沉淀
【2015年浙江省丽水市】在老师指导下,小科做了如下实验:点燃燃烧匙上的钠,迅速伸入盛有CO2的集气瓶中,盖上玻片,钠继续燃烧。反应结束后发现:集气瓶内壁附着黑色小颗粒,燃烧匙上粘附着灰白色固体。小科获知灰白色固体中的黑色固体成分是碳,但不清楚其中的白色固体成分是什么,于是进行了如下探究:
【提出问题】白色固体的成分是什么?
【建立假设】假设一:白色固体的成分是氧化钠;
假设二:白色固体的成分是碳酸钠;
假设三:白色固体的成分是氧化钠和碳酸钠的混合物。
【进行实验】
步骤1:取燃烧匙上灰白色固体于烧杯中,加入适量的水充分溶解,过滤,得到滤液;
步骤2:取少量步骤1中的滤液于试管中,滴加2滴酚酞试液,溶液变成红色。结论:白色固体的成分是氧化钠。有同学认为通过该实验得出的结论不正确,其理由是 。
步骤3:取少量步骤1中的滤液于试管中,滴加足量稀盐酸,溶液中有气泡冒出,结论是 。
步骤4:取少量步骤1中的滤液于试管中,加入过量的氯化钙溶液,出现白色沉淀,然后过滤,向所得滤液中滴加酚酞试液,无明显现象。则假设 成立。