下列实验设计方法正确的是
| A.向卤代烃加硝酸酸化的硝酸银来检验其中的卤族素元素 |
| B.实验用NH4Cl固体受热分解来制备NH3 |
| C.用盐酸和澄清石灰水来检验某物质是否含有CO32- |
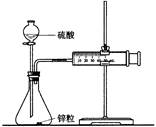
| D.可用下图所示的装置和药品来研究反应物浓度对反应速率的影响 |
甲醛(CH2O)、乙醛(CH3CHO)、丙醛(CH3CH2CHO)组成的混合物中,氢元素的质量分数为9%,则氧元素的质量分数为
| A.16% | B.37% | C.6% | D.不能确定 |
线型弹性材料“丁苯吡橡胶”的结构简式如下: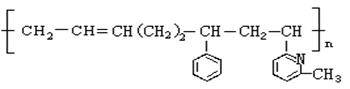
其单体可能是以下6种中的正确的组合是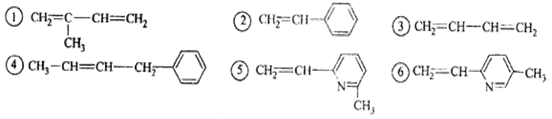
| A.②③⑥ | B.②③⑤ | C.①②⑥ | D.②④⑥ |
某烃和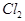 充分加成的产物结构简式为
充分加成的产物结构简式为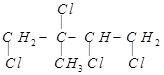 ,则原有机物一定是
,则原有机物一定是
| A.2—丁炔 | B.1,4—二氯—2—甲基—2—丁烯 |
| C.2—甲基—1,3—丁二烯 | D.1,3—丁二烯 |
已知化合物A (C4Si4H8) 与立方烷 (C8H8) 的分子结构相似,如下图: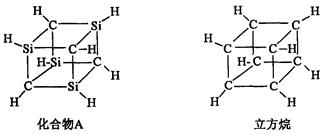
则C4Si4H8的二氯代物的同分异构体数目为
| A.3 | B.4 | C.5 | D.6 |
下列变化中,由加成反应引起的是
| A.乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色 |
| B.乙烯在一定温度、压强和催化剂的作用下,聚合为聚乙烯 |
| C.一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D.在催化剂作用下,由乙醇制取乙烯 |