NaOH能与CO2发生化学反应,其反应的化学方程式为________。然而,在化学课上老师向NaOH溶液通入CO2后无明显现象。提出问题:如何通过实验证明CO2与NaOH发生了反应。
【查阅资料】
①CaCl2溶液可与Na2CO3溶液发生复分解反应。
②向CaCl2溶液中通入CO2,无明显现象;在水溶液中CaCl2不与CO2、H2CO3等物质反应。
【实验一】证明反应物之一CO2消失了
(1)同学门设计了如图所示的实验,打开分液漏斗活塞。向充满CO2的广口瓶中滴入NaOH溶液。一会儿后可观察到的实验现象是___________________。并据此现象判断NaOH与CO2发生了化学反应。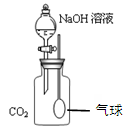
(2)老师提出上述实验不足以证明NaOH与CO2发生了化学反应。其理由是____________________。据此,你认为上述实验应做的改进是_____________________ 。
【实验二】证明有新物质Na2CO3生成
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案一:打开瓶塞,向实验一所得的溶液中加入饱和的石灰水,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。 方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
(1)写出方案二发生反应的化学方程式:___________________________。
(2)你认为上述实验方案不可行的是________,理由是______________________________。
(7分)某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察。请你一起参与分析,并完成后续实验设计。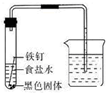
[观察现象]①装置中右侧导管中的液面升高。
②铁钉生锈,试管底部有黑色固体物质。
[提出问题]导管中液体为何升高?黑色固体物质又是什么?
[理论分析]小组同学根据已学过的知识分析得知,液面上升的原因是。
[猜想与假设]小组中的小明同学猜测该黑色固体可能含有:①Fe、②Fe2O3、③FeCl3、④C
四种物质。
[分析与验证]小组同学根据小明的四种猜测做了以下分析:
⑴小红同学认为不可能含有氯化铁,该结论得到小组同学的认可,理由是。
⑵小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是。
⑶小组同学不能确定是否含有铁,请人帮他们设计方案进行确认:
实验中学的小春和小玲同学在张老师的指导下,对呼吸作用是否产生CO2气体进行探究。请你一同参与:
【提出问题】人呼出的气体中是否含有CO2气体?
【设计方案并实验】
小春:在试管中加入2 mL蒸馏水,用玻璃导管向其中吹气,未发现明显现象。
小玲:在试管中加入2 mL澄清石灰水,用玻璃导管向其中吹气,溶液变浑浊。
【解释与结论】小玲的实验结果证实了呼出的气体中含有CO2气体,其方案中的实验
原理可用符号表达式表示为___________________________________。
【评价与反思】小春的实验若继续进行,也能得到与小玲相同的结论。请你帮助设计后续方案:实验操作为_________________________________________________;实验现象是________________________________________________________。
有 和 混合物l8.6g。为测定其中 的质量,将固体溶于水,并逐渐加入稀硫酸至100g时,开始产生气体;再加入稀硫酸至100g时,不再产生气体,生成气体共4.4g(提示: )
(1)在图28中画出产生气体的质量与所加稀硫酸质量的关系曲线。
(2)求混合物中
的质量是多少?
(3)所用稀硫酸的溶质质量分数是多少?
在查阅资料时,小明得知
在高温条件下能与木炭反应生成
。他决定对该反应进行探究。
[提出问题]
与木炭在高温条件下反应是否生成
?
[实验探究]小胡设计了如图的实验方案,并进行实验。
(1)
中用石灰石与稀盐酸反应生成
,反应的化学方程式为。
(2)
中装有饱和碳酸氢钠溶液,其作用是除去
气体中混有的少量
气体。
中装有浓硫酸。其作用是。
(3)
中装入氢氧化钠溶液的作用是。
[实验结论]经检验
处的气体为
。结论:
在高温条件下与木炭反应生成了
。
[实验反思] (4)有同学对
装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是。
[实验拓展] (5)撤去
,按
顺序连接。然后
中用二氧化锰和过氧化氢溶液混合生成
,反应的化学方程式为。此时要检验该实验条件下
中木炭所发生反应的生成物,还需要补充和完善的实验是。
小军家的下水管道堵了。爸爸买回一种"管道通",使用后堵塞的管道畅通无阻了。小军对此很好奇,于是想探究"管道通"中的物质成分。
【提出问题】"管道通"中的物质是什么?
【查阅资料】主要内容如下。
(1)下水管道里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱 ,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体。铝与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是。
②铝与氢氧化钠溶液反应的化学方程式是.
【猜想与验证】小军打开一盒"管道通",内有一袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
| 实验操作 |
实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿。 |
。 |
| ②将适量白色固体颗粒放入盛有适量水的试管中,并用手触摸试管外壁。 |
试管外壁发烫。 |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间。 |
羊毛线逐渐消失。 |
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
| 实验操作 |
实验现象 |
 ①按照下图安装两套仪器。 ①按照下图安装两套仪器。 |
|
| ②一套仪器中加入银灰色粉末和稀盐酸;另一套仪器中加入银灰色粉末、。 |
都产生大量无色气体,试管外壁温度明显升高。 |
| ③待导管口有气泡均匀持续冒出时,分别收集1试管气体,验纯。 |
用拇指堵住试管口,移近酒精灯火焰,松开拇指,发出轻微的。 |
| ④在导管口点燃气体。 |
火焰颜色为。 |
【结论】银灰色粉末为铝粉。
【应用】使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口。一会儿,管道内发生化学反应。根据题目信息,推测管道内的反应现象是。
【反思】①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似。要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在。
②根据本实验分析,使用"管道通"时,应注意的事项有(填一条即可)。