下面A~F是几种常见烃的分子球棍模型。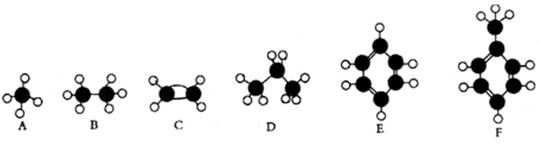
根据上述模型,回答下列问题:
(1)常温下含碳量最高的液态烃是 。
(2)能够发生加成反应的气态烃是 。
(3)一氯代物的同分异构体最多的是 。
(4)所有原子均在同一平面上的是 。
(5)能使酸性高锰酸钾溶液褪色的是 (填对应字母)。
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g) 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度 |
450 |
500 |
550 |
600 |
| SO2的转化率% |
97.5 |
95.8 |
90.50 |
80.0 |
(1)由表中数据判断△H 0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是
A容器的压强不变 B混合气体的密度不变
C混合气体中SO3的浓度不变 D C(SO2)=C(SO3)
E V正(SO2)=V正(SO3) F V正(SO3)=2V逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1.
①0~2min之间,O2的反应速率为 .
②此时的温度为 ℃.
③此温度下的平衡常数为 (可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将 向移动.
如图,外接电源为Zn-MnO2干电池,甲、乙为相互串联的两个电解池,请回答:
(1)甲池若为用电解原理精炼铜的装置,
B电极是 极,材料 A电极反应式为 ,
电解质溶液可以是
(2)乙池中Fe极是 极,若滴入少量酚酞试液,开始一段时间后,Fe极附近呈 色,若C电极
材料为石墨,C电极反应式为
(3)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。该电池的负极材料是 ,电极反应式为 。
(1) 2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
请回答下列问题: ①图中A点表示:
①图中A点表示:
C点表示:
E的大小对该反应的反应热 (填“有”或“无”)影响。 ②图中△H= 。
②图中△H= 。
( 2 )由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:
②若1 mol水蒸气转化为液态水放热45kJ,则反应H2(g) + O2(g) = H2O( l )的ΔH= 。氢气的燃烧热为ΔH= 。
O2(g) = H2O( l )的ΔH= 。氢气的燃烧热为ΔH= 。
2015年“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫:(请用图中物质前的序号连接起来表示所走的路线)______________。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有______个,属于氧化还原反应的有____个。其中能“吃掉”盐酸的盐是__________(填物质名称),写出该反应的离子方程式_______________;
(3)在不能与盐酸反应的物质中,属于电解质的是__________ (填写物质序号)。
Ⅰ、下表中括号内物质是杂质,试将除杂试剂及分离方法填入表内:
| 混合物 |
Fe ( Al) |
H2O(I2) |
| 除杂试剂 |
||
| 除杂方法 |
Ⅱ、等温等压下,等体积的O2和O3所含分子个数比为________, 质量之比为________。
Ⅲ、将适量的铁粉加入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+的物质的量浓度相等,则已反应的Fe3+和原溶液中的Fe3+的物质的量之比为 ;将绿豆大一粒钠投入硫酸铜溶液中,写出总的化学方程式 。