【化学--选修3物质结构与性质】
铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
①Cu2+的价电子排布图 ; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
② 的空间构型为_____________,
的空间构型为_____________, 离子中心原子的杂化方式为 。
离子中心原子的杂化方式为 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式: 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因 .
(4)Cu晶体的堆积方式如图所示,设Cu原子半径为r,
晶体中Cu原子的配位数为_______,晶体的空间利用率
为 (  ,列式并计算结果)。
,列式并计算结果)。
合成氨尿素工业生产过程中涉及到的物质转化过程如下图所示。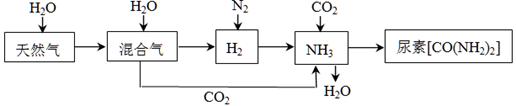
(1)天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为。
(2)甲烷是一种清洁燃料,但不完全燃烧时热效率降低,同时产生有毒气体造成污染。
已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) ΔH1=―890.3 kJ/mol
2CO (g) + O2(g)=2CO2(g) ΔH2=―566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率是完全燃烧时的_____倍(计算结果保留1位小数)。
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的正极反应式是________。
②当线路中有0.1 mol电子通过时,________(填“a”或“b”)极增重________g。
(4)运输氨时,不能使用铜及其合金制造的管道阀门。因为在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成[Cu(NH3)4]2+,该反应的离子方程式为。
已知甲和乙在溶液中的转化关系如图所示:
请回答下列问题:
(1)若甲是10电子的单核微粒,乙是两性氢氧化物,则微粒甲的结构示意图为 。
(2)若甲是10电子的阳离子,乙是碱性气体。1mol乙通入足量强酸溶液中与H+反应,反应过程中能量变化如下图: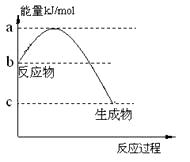
写出乙的一种用途: ;
该反应的热化学方程式是___________________________。
(3)若甲是CrO42-(黄色)和Cr2O72-(橙色)的混合溶液,在该溶液中存在如下平衡:
CrO42-(黄色) + 2H+ Cr2O72-(橙色) + H2O
Cr2O72-(橙色) + H2O
若测得甲溶液的pH=1,该溶液显 色。
(4)若甲仅含有NO3-、SO42-和X三种离子,则X离子可能是 (填序号) 。
| A.Fe2+ | B.HCO3- | C.Ba2+ | D.Fe3+ |
(5)若甲是CO2,乙中HCO3-和CO32-的物质的量浓度相等,此时溶液的pH=10,
则HCO3-的电离平衡常数Ka= 。
油脂A的通式为 (R中不含有三键)0.1 mol A与溶有96 g Br2的四氯化碳溶液恰好完全反应.0.1 mol A完全燃烧时生成的CO2和H2O的物质的量之和为10.6 mol.求油脂A的结构简式,写出油脂A完全氢化的化学方程式.
(R中不含有三键)0.1 mol A与溶有96 g Br2的四氯化碳溶液恰好完全反应.0.1 mol A完全燃烧时生成的CO2和H2O的物质的量之和为10.6 mol.求油脂A的结构简式,写出油脂A完全氢化的化学方程式.
一种有机物的结构简式为: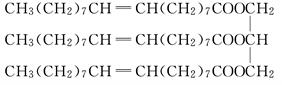
完成下列问题:
(1)该化合物含有的官能团是________(填名称).
(2)该化合物的类别是________(填字母序号,下同).
A.烯烃 B.酯 C.油脂 D.高分子化合物
E.混合甘油酯
(3)该化合物与水的混合物________.
A.与水互溶
B.不溶于水,水在上层
C.不溶于水,水在下层
(4)该物质是否有固定熔、沸点________(填“是”或“否”).
(5)与该物质能反应的物质有________.
A.NaOH溶液 B.碘水 C.乙醇 D.乙酸 E.H2
写出属于取代反应的化学方程式:
________________________________________________________________________.
如图为硬脂酸甘油酯在碱性条件下水解的装置图.
进行皂化反应时的步骤如下:
(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g氢氧化钠、5 mL水和10 mL酒精.加入酒精的作用是______________.
(2)隔着石棉网给混合物加热约10 min,皂化反应基本完成,所得的混合物为________(填“悬浊液”、“乳浊液”、“溶液”或“胶体”).
(3)向所得混合物中加入________,静置一段时间,溶液分为上下两层,肥皂在________层,这个操作称为________.
(4)图中长玻璃导管的作用为__________________________________________.
(5)写出该反应的化学方程式:__________________________________.