(10分,每空2分) 往一个容积为5L的密闭容器中,通入2molN2和3molH2,在一定条件下,发生反应 N2+3H2 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求:
(1)2 min时,N2的物质的量 ; (2)2 min时,H2的物质的量浓度 ;
(3)2 min时,H2的转化率 ; (4)2min内,N2的平均反应速率 ;
(5)N2、H2、NH3的反应速率之比 。
现有下列九种物质:①H2②铝③CuO④CO2⑤稀H2SO4⑥稀硝酸 ⑦氨水⑧Ba(OH)2固体 ⑨熔融Al2(SO4)3,用序号回答下列问题。
(1)上述物质中,属于碱的是。
(2)上述物质或溶液中若两两反应的离子方程式为:H++OH— H2O,则对应的两种物质是。
H2O,则对应的两种物质是。
(3)上述物质或其溶液若两两反应生成氢气,则对应的两种物质的组合分别是。
(4)17.1g⑨溶于水配成250mL溶液, SO42-的物质的量浓度为。
(5)在⑧的溶液中通入过量的④,写出总反应的离子方程式。
(6)在特殊条件下,②与⑥发生反应的化学方程式为:8Al + 30HNO3 = 8Al(NO3)3 +3X + 9H2O,该反应中X的化学式是,其中还原剂与氧化剂的物质的量之比是,当有8.1g Al发生反应时,转移电子的物质的量为。
某课题组研究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺,其设计的流程如下:
回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式;
(2)“酸溶”中反应的离子方程式为;
(3)“过滤”后滤液中金属阳离子有;
(4)“氧化”中使用的氧化剂最好是;
(5)该工艺流程中产生的SO2会污染空气并形成酸雨,下列物质:①BaCl2②品红③石灰乳 ④O2,用于吸收SO2最好的是。
下图是氮元素的各种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A的摩尔质量是,从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有。
(2)实验室依据复分解反应原理制取NH3的化学方程式是。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使。
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为。
(5)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的,若开始时投入17吨NH3,最后生产出的硝酸为42吨,则硝酸的产率是。
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。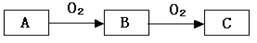
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,试用化学方程式表示该物质与二氧化碳气体的反应 。将C长期露置于空气中,最后将变成物质D,D的化学式为 。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题:
①收集A的方法是 ,验证A是否已经收集满的方法是 (任写一种)。
②写出实验室制取A的化学方程式 。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
④试写出C与水反应的化学方程式 ,反应可得到酸X,X是 电解质(填“强”或“弱”)。如下图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式 。实验完毕后,试管中收集到的气体的主要成分为 (写化学式)。
(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:________________。
(2)有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl五种物质中的某几种组成,现进行如下实验:
①将白色粉末加水溶解,得无色溶液。
②向①中所得的无色溶液中加入NaOH溶液,观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B。
根据上述现象判断:
①A的化学式是 B的化学式是 。
②原白色粉末中一定含有 ,可能含有 ,对可能含有的物质,可通过 (填实验名称)进一步检验。检验操作步骤有:①蘸取待测液②置于酒精灯火焰上灼烧 ③透过蓝色钴玻璃观察 ④用稀盐酸洗净铂丝。其中正确的操作顺序为 。
A.①②③④ B.④①②③ C.④②①②③④ D.①③②④