(18分)化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:
已知以下信息:① A的核磁共振氢谱表明其只有一种化学环境的氢;
②R—CH=CH2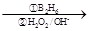 R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的结构简式为 ,B所含官能团的名称是 。
(2)C的名称为 ,E的分子式为 。
(3)A→B、C→D、F→G的反应类型分别为 、 、 。
(4)写出下列反应的化学方程式;
D→E第①步反应 ;
F→G 。
(5)I的结构筒式为 。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有 种(不考虑立体异构)。J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式 。
向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:
(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为____________mol(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5mol(L·min);乙:ν(Y)=2mol(L·min);丙:ν(Z)=4.5mol(L·min);丁:ν(X)=0.075mol(L·s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)________________。
(3)若向达到(1)的平衡体系中充入氮气,则平衡 向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。
向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比___
| A.无法确定 | B.前者一定大于后者 |
| C.前者一定等于后者 | D.前者一定小于后者 |
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则a、b、c应满足的关系为____________。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则起始时维持化学反应向逆反应方向进行,则c的取值范围应为______________。
(6分)(1)P4(白磷,s)+5O2(g)=P4O10(s)ΔH=-2983.2kJ/mol
(2)P(红磷,s)+5/4O2(g)=1/4 P4O10(s)ΔH=-738.5kJ/mol
则白磷转化为红磷的热化学方程式为___________________。相同状况下,能量较低的是______;红磷的稳定性比白磷____
(10分)A~H是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色。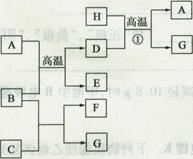

请回答下列问题:
(1)元素B在周期表中的位置是,C的电子式为,H的结构式为。
(2)反应①的化学方程式为。
(3)A与盐酸反应的离子方程式为。
(4)F溶液显(填“酸性”、“中性”或“碱性”),原因是(用离子方程式表示)。
(10分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中
溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为。
(2)丙池中F电极为(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应
方程式为。
(3)当乙池中C极质量减轻10.8 g时,甲 池中B电极理论上消耗O2的体积为mL(标准状况)。
池中B电极理论上消耗O2的体积为mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(0H)2CO3 |
(12分)科学家一直致力于“人工固氮”的方法研究。
(1)合成氨的原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g) H=-92.4 kJ/mol,该反应的能量变化如图所示。
H=-92.4 kJ/mol,该反应的能量变化如图所示。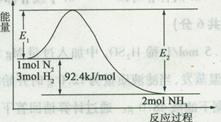
①在反应体系中加入催化剂,反应速率增大,E2的变化是(填“增大”、“减小”或“不变”)。
②将0.3 mol N2和0.5 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的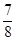 ,此时H2的转化率为;欲提高该容器中H2的转化率,下列措施可行的是(填选项字母)。
,此时H2的转化率为;欲提高该容器中H2的转化率,下列措施可行的是(填选项字母)。
| A.向容器中按原比例再充入原料气 | B.向容器中再充入一定量H2 |
| C.改变反应的催化剂 | D.液化生成物分离出氨 |
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生反应:
2N2(g)+6H2O(1) 4NH3(g)+3O2(g)
4NH3(g)+3O2(g) H="+1530" kJ/mol
H="+1530" kJ/mol
又知:H2O(1)=H2O(g) H=+44.0 kJ/mol
H=+44.0 kJ/mol
则2N2(g)+6H20(g) 4NH3(g)+302(g)
4NH3(g)+302(g) H =kJ/mol,该反应的化学平衡常数表达式为K=,控制其他条件不变,增大压强,K值(填“增大”、“减小”或“不变”)。
H =kJ/mol,该反应的化学平衡常数表达式为K=,控制其他条件不变,增大压强,K值(填“增大”、“减小”或“不变”)。