关于下列各图的说法中,正确的是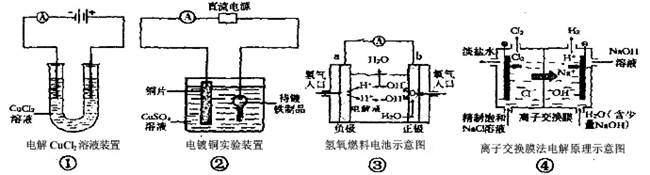
| A.①中与电源负极相连的电极附近能产生使湿润淀粉KI试纸变蓝的气体 |
| B.②中待镀铁制品应该与电源的正极相连接 |
| C.③中的b极是电子流出的极,发生氧化反应 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
有关Na2CO3和NaHCO3的叙述中正确的是 ()
| A.Na2CO3和NaHCO3均可与NaOH溶液反应 |
| B.NaHCO3比Na2CO3热稳定性强 |
| C.相同物质的量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体的量相同 |
| D.相同质量的Na2CO3和NaHCO3与足量盐酸作用时,二者消耗的盐酸一样多 |
下列由实验现象得出的结论正确的是:()
| A.向某无色液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有Ag+ |
| B.向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32﹣ |
| C.加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华 |
| D.向NaBr溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈橙红色,说明Br-还原性强于Cl- |
下图是某些实验的部分装置,其中所注明的实验能达到实验目的的( )
将赤铜矿(Cu2O)与辉铜矿(Cu2S)混合加热发生以下反应:Cu2S+2Cu2O 6Cu+SO2↑,下列说法错误的是()
6Cu+SO2↑,下列说法错误的是()
| A.在Cu2O、Cu2S中Cu元素化合价都是+1价 |
| B.反应中Cu元素被氧化,S元素被还原 |
| C.Cu2S在反应中既是氧化剂,又是还原剂 |
| D.每生成6.4g Cu,反应中转移0.2 mole- |
向下列溶液中逐渐通入SO2,一直不产生沉淀的是()
| A.Ca(OH)2溶液 | B.CaCl2溶液 |
| C.Ba(NO3)2溶液 | D.H2S的水溶液 |