硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。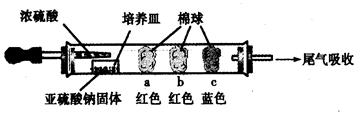
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:
| 棉球 |
棉球上滴加的试剂 |
实验现象 |
解释和结论 |
| a |
|
棉球变白,微热后又恢复红色 |
|
| b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式: |
| c |
|
棉球变为白色 |
该气体具有 (选填“氧化性”或“还原性”) |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。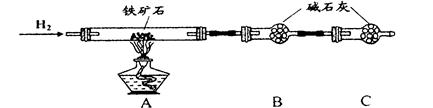
实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定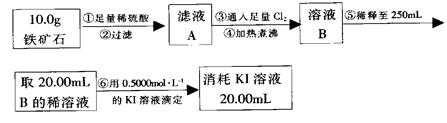
(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
A.滴定管用蒸馏水洗涤后再用待装液润洗
B.锥形瓶需要用待测液润洗
C.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
有A、B、C、D、E、F、G 7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。
| A |
B |
C |
D |
E |
F |
G |
|
| A |
- |
- |
- |
- |
- |
- |
↓ |
| B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
| C |
- |
- |
- |
↓ |
- |
↓ |
↓ |
| D |
- |
- |
↓ |
- |
↓ |
↓ |
↓ |
| E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
| F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
| G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
试完成下列问题。
(1)A的化学式是_____________,G的化学式是_____________。判断理由是
_______________。
(2)写出其余几种物质的化学式。B: _____________,C: _____________,D: _____________,E: _____________,F: _____________
今有下列两组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。两组物质分别为:
(1)NaCl、BaCO3、AgNO3、蔗糖
(2)BaSO4、K2CO3、Na2CO3、(NH4)2CO3
| 组别 |
被选出的物质 |
分类依据 |
| 第(1)组 |
||
| 第(2)组 |
一定条件下,在体积为3 L的密闭容器中反应CO(g)+ 2H2(g) CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。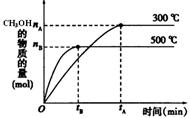
(1)该反应的平衡常数表达式K=;根据右图,升高温度,K值将(填“增大”、“减小”或“不变”)。
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是(填字母)。
a. v生成(CH3OH)= v消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变d. CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是(填字母)。
a.c(H2)减少 b正反应速率加快,逆反应速率减慢
c. CH3OH的物质的量增加d.重新平衡时c(H2)/ c(CH3OH)减小
下表是元素周期表的一部分,表中所列字母分别代表短周期中的一种元素:
| A |
B |
||||||
| C |
D |
(1)A单质电子式是;B元素在周期表中的位置是。
(2)D单质与C的最高价氧化物对应水化物反应的离子方程式是。
(3)A的气态氢化物与其最高价氧化物对应水化物反应所得产物的名称是,该产物对水的电离起促进作用的原因是。
(17分)阿魏酸在医药、保健品、化妆品原料和食品添加剂等方面有着广泛的用途,其
结构简式为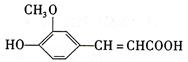
⑴阿魏酸可以发生 (填选项字母)。"
a.酯化反应 b.消去反应 c.加成反应 d.氧化反应 e.银镜反应
⑵阿魏酸的一种同分异构体A 可用于制备有机玻璃(聚甲基丙烯酸甲酯),转化关系如下图所示: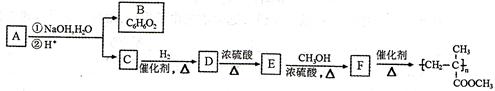
己知A 和B都能与FeCl3溶液发生显色反应,B的一溴代物只有一种,A、C能发生银镜反应。
①B的结构简式为____________,C含有的官能团为____________。
②D→E的化学方程式为____________________________________。
③A的结构简式为__________________________________________。
(3)写出所有符合下列条件的阿魏酸的同分异构体的结构简式。
①苯环上有两个取代基,且苯环上的一漠代物只有2 种;
②能发生银镜反应;
③与碳酸氢钠溶液反应可放出使澄清石灰水变浑浊的气体;
④与FeCl3溶液发生显色反应__________________________________________。