(共8分)(1)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e-―→2O2-)。
(1) ①c电极的名称为________,d电极上的电极反应式为 。
②如图2所示电解100mL 0.5mol·L-1 CuSO4溶液。若a电极产生56mL(标准状况)气体,则所得溶液的pH=_____(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入______(填字母序号)。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(2)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在a~c装置中,能保护铁的是________(填字母)。
②若用d装置保护铁,X极的电极材料应是________(填名称)。
下表是某品牌食品包装袋上的说明
| 品名 |
肉松蛋卷 |
| 配料 |
小麦粉;②鸡蛋;③食用植物油;④白砂糖⑤肉松; ⑥食用盐; ⑦食用香料; ⑧β-胡萝卜素;⑨苯甲酸钠 |
| 生产日期 |
标于包装袋封口上 |
(1)配料中的着色剂是 (填序号)
(2)蛋白质是重要营养物质,处于生长发育期的青少年需要量很大。上述配料中,富含蛋白质的是
________。(填序号)
(3)食用植物油摄入人体后,在酶的作用下水解为高级脂肪酸和 (写名称),进而被氧化成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(4)该食品配料中还缺少的营养素是 (填名称);为均衡营养,可在食用该“肉松蛋卷”时,最好配以下列食品中的 (填标号)
A.牛肉 B.菠菜 C.马铃薯(土豆)
.有甲、乙、丙三种物质: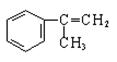
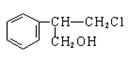

甲乙丙
(1)乙中含有的官能团的名称为____________________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):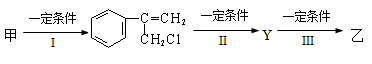
其中反应I的反应类型是_________,反应II的条件是_______________,反应III的化学方程式为__________________________________(不需注明反应条件)。
(3)由甲出发合成丙的路线之一如下: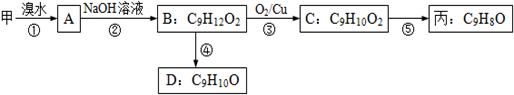
(a)下列物质不能与B反应的是(选填序号)。
a.金属钠 b.FeCl3c.碳酸钠溶液 d.HBr
(b)丙的结构简式为。
(c)任写一种能同时满足下列条件的D的同分异构体结构简式。
a.苯环上的一氯代物有两种
b.遇FeCl3溶液发生显色反应
c.能与Br2/CCl4发生加成反应
(10分)根据下面各物质之间的转化关系,回答问题: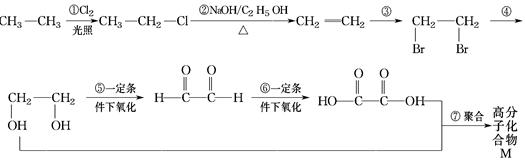
(1)属于取代反应的有(填序号,下同)___________,属于加成反应的有 _________。
(2)写出反应③、④的化学方程式(有机物用结构简式表示,注明反应条件,下同)
a.反应③___________________________________________________________。
b.反应④__________________________________________________________。
(3)写出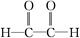 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
___________________________________________________________________。
(4分)取14.3gNa2CO3•XH2O溶于水配成100mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸20.0mL,并收集到1.12LCO2(标准状况)。试计算:
(1)稀盐酸物质的量浓度为 mol/L;
(2)x值是。
(4分)拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能。下表是某些共价键的键能:
| 共价键 |
H-H |
O=O |
H-O |
| 键能/kJ ·mol-1 |
436 |
498 |
X |
根据下图中能量变化图,回答下列问题: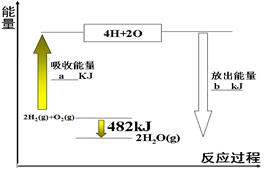
(1) 图中:a=___________。
(2) 表格中:X=。