某化学课外研究小组拟对一种焰火原料(由两种短周期中的常见金属元素的单质组成的合金粉末)进行探究。请完成下列探究报告。
【探究目的】探究该焰火原料的组成
【资料检索】Mg2+检验的方法:取 2 滴待检液,加入 2 滴 2mol/LNaOH 溶液,再加入 2 滴镁试剂(I)染料(对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(I)染料呈天蓝色,表示待测液中含有 Mg2+。注:Ag+、Cu2+、Fe3+、NH4+会妨碍 Mg2+的检测,Mg(OH)2可溶于 浓的氯化铵溶液,其他的常见不溶性碱难溶于氯化铵溶液。
【探究思路】确定该焰火原料所含金属种类
【实验探究】
(1)甲同学进行了初步试验,实验步骤和实验现象如下。请填写下表。
| 序号 |
实验步骤 |
实验现象 |
结论 |
| ① |
取少量该焰火原料,加入冷水 |
无明显现象 |
|
| ② |
取少量该焰火原料,加入稀盐酸 |
完全溶解,大量气体产生、溶液呈无色 |
|
(2)乙同学取甲同学第②组实验的溶液,加入镁试剂(I)染料,未见天蓝色物质。他得出合金中不含镁离子的结论。乙同学的结论(填“正确”或“错误”)你的理由是
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下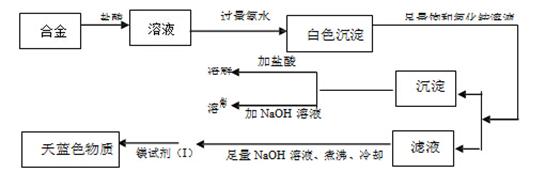
由丙同学的实验记录可知该焰火原料是由 和 两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸的理由是
(8分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。实验室可以用装置F制备氯气
请回答下列问题:
(1)装置F中发生反应的离子方程式为_____________________________;
(2)为了快速制备氨气,装置A的烧瓶中可装试剂____________________;
(3)E装置的作用是_______,DE的位置能不能调换(填“能”或“不能”);
(4)通入C装置的两根导管左边较长、右边较短,目的是_______________;
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:__________________________________。
某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
A. 浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色。 |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 |
B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,产生大量无色气体。 |
| 4.将镁条投入稀盐酸中 |
D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 |
E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等。
仪器:①,试管,试管夹,烧杯,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(将与实验步骤对应的实验现象的编号和离子方程式填在答题卷上)
(4)实验结论:。
无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等。某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤。除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体。
①加入少量氧化锌调节滤液使pH≈2目的是;
②加热蒸发、浓缩溶液时,应加热到时,停止加热。
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解。停止加热,让其自然冷却、结晶。抽滤(装置如图所示)。将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体。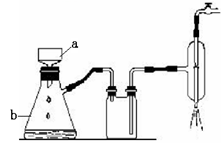
①写出下列仪器的名称。a ;b
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是。
③用少量无水乙醇洗涤晶体的目的是。
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量(填“有”、“无”)影响,原因是。
氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN—等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
I.查阅资料:含氰化物的废水破坏性处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
II.实验验证:破坏性处理CN-的效果。
化学兴趣小组的同学在密闭系统中用图10装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol·L—1)倒入甲中,塞上橡皮塞。
步骤3:
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式。
(2)完成步骤3。
(3)丙装置中的试剂是,丁装置的目的是。
(4)干燥管Ⅱ的作用是。
(5)请简要说明实验中通入N2的目的是。
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为。
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。请你帮助该同学整理并完成实验报告:
| 实验方案 |
实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 |
(A)浮于水面,熔成小球,在水面上游动,随之消失,溶液变红 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 |
(B)产生气体,可在空气中燃烧,溶液变为浅红色 |
| ③钠与滴有酚酞试液的冷水反应 |
(C)反应不十分强烈,产生的气体可在空气中燃烧 |
| ④镁带与2mol/L盐酸反应 |
(D)剧烈反应,产生可燃气体 |
| ⑤铝条与2mol/L盐酸反应 |
(E)生成白色胶状沉淀,后来沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 |
(F)生成淡黄色沉淀 |
(1) 实验目的: 研究同周期元素性质递变规律
(2) 实验用品:
仪器: ①________②________③________④ 试管夹 ⑤ 镊子 ⑥ 小刀 ⑦ 玻璃片⑧ 砂纸等;
药品:钠、镁带、铝条、2mol/L的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等。
(3) 实验内容:(填写与实验方案相对应的实验现象)
①______②______③______④______⑤______⑥______(用A-F表示)
(4) 实验结论:
金属性: ________________非金属性: ________________
(5)写出⑥的离子方程式:_________________________________。