[化学一选修3:物质结构与性质]
(1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未 成对的电子,w的原子序数为29。回答下列问题:
①Y2X2分子中Y原子轨道的杂化类型为_________,1molY2X2含有 键的数目为____ __________________.
键的数目为____ __________________.
②化合物ZX3的沸点比化台物YX4的高,其主要原因是_____________。
③元素Y的一种氧化物与元素z的一种氧化物互为等电子体,元素z的这种氧化物的分子式是_____________。
(2)铁元素能形成多种配合物,如:Fe(CO)x
①基态Fe3+的M层电子排布式为___________________________。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18.则x=_________。常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(填晶体类型):
(3)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_________。已知该晶胞的密度为 g/cm
g/cm ,阿伏加德罗常数为
,阿伏加德罗常数为 ,求晶胞边长a=________cm。(用含
,求晶胞边长a=________cm。(用含 的计算式表示)
的计算式表示)
(4)下列有关的说法正确的是_____________。
| A.第一电离能大小:S>P>Si |
| B.电负性顺序:C<N<O<F |
| C.因为晶格能Ca0比KCl高,所以KCl比CaO熔点低 |
| D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大 |
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
在一定温度下,把2 mol N2和6 mol H2通入一个体积不变的密闭容器中,(如图)
容器中发生以下的反应:N2(g)+3H2(g)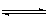 2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a="1" mol ,c="2" mol ,则b="____" mol,在此情况下,反应起始时将向方向进行(填“正”或“逆”)
(2)若规定起始时反应向逆反应方向进行,则c的范围是。
(3)在上述装置中,若需控制平衡后的混和气体的物质的量为6.5 mol,则可采取的措施是
某温度时,A+B 2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。
2C反应达到平衡状态,如果A为气体,且压强增大时,A的平衡浓度增大,则B为_________态或__________态,C为________态;如果减少或增加B的量,平衡不移动,则B是__________态;如果降温,C的平衡浓度降低,此反应的逆反应是___________热反应。
(10分)在一密闭容器中发生反应N2+3H2 2NH3.达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
2NH3.达到平衡后,只改变某一个条件时,反应速率与反应进程的关系如图所示:
回答下列问题:
(1)处于平衡状态的时间段是(填选项);
(2)t1 t2 t3时刻分别改变的一个条件是(填选项)
A 增大压强B、减小压强 C.升高温度
D、降低温度 E、加催化剂F、充人氮气
t1时刻 t3时刻 t4时刻
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是(填选项);
(4)如果在t6对刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化情况;
(5)一定条件下,合成氨反应达到平衡时,测得反应混合气中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为
X,Y,Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应:Y+X→A(g),Y+Z→B(g)。请针对以下两种不同情况回答:
(1)若常温下X,Y,Z均为气体,A的相对分子质量大于B,且A和B化合生成固体C时有白烟产生,则:①C的电子式是__________;②B溶于水的过程中存在的可逆反应式为___________________________。
(2)若常温下Y为固体,X,Z为气体,A在空气中充分燃烧可生成B,则:①A的化学式是_________;②向苛性钠溶液中通入过量的B,所发生反应的离子方程式是_______________________。③若A的燃烧热为M kJ·mol-1,试写出该反应的热化学方程式_____________________
(1)实验室制NH3的反应方程式为_____________________________________
(2)氨的催化氧化是工业制取硝酸的基础,写出化学反应方程式。
(3)硝酸具有强氧化性,它能和许多物质发生反应。写出浓硝酸与非金属单质碳的反应方程式。
(4)写出稀硝酸与金属银在加热条件下的反应方程式 _______________________________________________________